题目内容
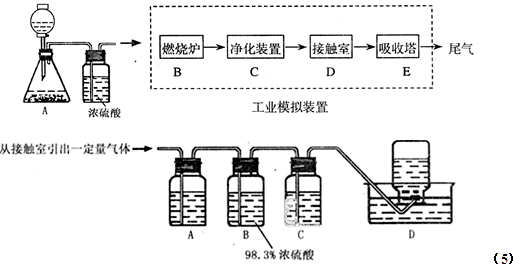
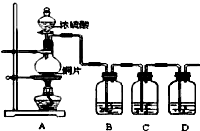 某化学兴趣小组的同学为探究二氧化硫的化学性质,设计了如图所示的装置.
某化学兴趣小组的同学为探究二氧化硫的化学性质,设计了如图所示的装置.请回答下列问题.
(1)铜和浓硫酸反应的化学方程式为
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
| ||
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
.
| ||
(2)B瓶中盛有品红溶液,观察到品红溶液褪色,这是因为 SO2具有
C
C
(填选项的字母,下同),C瓶中盛有新制的氯水,观察到氯水褪色,这是因为SO2具有B
B
.A.氧化性 B.还原性 C.漂白性
(3)D瓶中盛有NaOH溶液,作用是
吸收尾气,防止污染
吸收尾气,防止污染
.(4)充分反应后,小组同学发现铜和硫酸都有剩余.若想使剩余的铜片溶解,可再加入(多选)
ABC
ABC
(填选项的字母).A.HNO3 B.NaNO3 C.Fe2O3 D.Na2CO3.
分析:(1)铜和热的浓硫酸反应生成二氧化硫、硫酸铜和水;
(2)二氧化硫与品红作用,二氧化硫具有漂白性;二氧化硫与氯水作用,二氧化硫具有还原性;
(3)铜和热的浓硫酸反应,生成的二氧化硫为大气污染物,氢氧化钠和二氧化硫反应生成亚硫酸钠和水;
(4)加氧化性物质与稀硫酸在同一溶液,能氧化铜单质.
(2)二氧化硫与品红作用,二氧化硫具有漂白性;二氧化硫与氯水作用,二氧化硫具有还原性;
(3)铜和热的浓硫酸反应,生成的二氧化硫为大气污染物,氢氧化钠和二氧化硫反应生成亚硫酸钠和水;
(4)加氧化性物质与稀硫酸在同一溶液,能氧化铜单质.
解答:解:(1)铜和热的浓硫酸反应铜作还原剂,硫酸作氧化剂,生成二氧化硫、硫酸铜和水,
故答案为:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O;
(2)二氧化硫与品红溶液反应生成不稳定的无色物质,二氧化硫与品红作用,二氧化硫具有漂白性;二氧化硫具有还原性,能被氯水氧化,氯水褪色,发生O2+C12+2H2O=H2SO4+2HC1,
故答案为:C;B;
(3)SO2是酸性氧化物,也是大气污染物,所以用NaOH溶液吸收,氢氧化钠和二氧化硫反应生成亚硫酸钠和水,反应的方程式为:2NaOH+SO2=Na2SO3+H2O,
故答案为:吸收尾气,防止污染;
(4)铜和浓硫酸反应时,当硫酸稀到一定程度时,该反应停止,可以加入氧化剂,铜能继续溶解,如NaNO3与稀硫酸在同一溶液相当于稀硝酸,稀硝酸能和铜单质在常温下反应,Fe2O3溶于稀硫酸生成氧化性的三价铁能和铜反应,
故答案为:ABC.
故答案为:Cu+2H2SO4(浓)
| ||
(2)二氧化硫与品红溶液反应生成不稳定的无色物质,二氧化硫与品红作用,二氧化硫具有漂白性;二氧化硫具有还原性,能被氯水氧化,氯水褪色,发生O2+C12+2H2O=H2SO4+2HC1,
故答案为:C;B;
(3)SO2是酸性氧化物,也是大气污染物,所以用NaOH溶液吸收,氢氧化钠和二氧化硫反应生成亚硫酸钠和水,反应的方程式为:2NaOH+SO2=Na2SO3+H2O,
故答案为:吸收尾气,防止污染;
(4)铜和浓硫酸反应时,当硫酸稀到一定程度时,该反应停止,可以加入氧化剂,铜能继续溶解,如NaNO3与稀硫酸在同一溶液相当于稀硝酸,稀硝酸能和铜单质在常温下反应,Fe2O3溶于稀硫酸生成氧化性的三价铁能和铜反应,
故答案为:ABC.
点评:本题主要考查了铜和浓硫酸的反应,综合性强,关键在于掌握铜和浓硫酸反应的方程式和产物的检验,题目难度中等.

练习册系列答案
相关题目