题目内容
【题目】有机物M可从酸牛奶中提取。已知纯净的M为无色黏稠液体, 易溶于水。为研究M的组成与结构,进行了如下实验:
实验步骤 | 解释或实验结论 |
(1)称取M4.5 g,升温使其汽化,测其密度是相同条件下H2的45倍。 | 试通过计算填空:(1)M的摩尔质量为: __ 。 |
(2)将此4.5 g M 在足量纯 O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重2.7g和6.6 g | (2)M的分子式为:____ 。 |
(3)通过M 的红外光谱图发现该分子中既有 羟基,还有羧基 | (3)写出M中含有的官能团羟基电子式:__ |
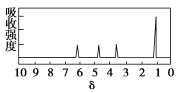
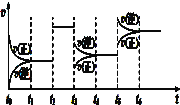
(4)M 的核磁共振氢谱如下图:
| (4)M 中含有___种氢原子。 |
(5)综上所述,M 的结构简式为_____ 。 | |
【答案】 90g/mol C3H6O3 ![]() 4
4 ![]()
【解析】试题分析:根据相同条件下密度比等于摩尔质量之比计算;产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重2.7g和6.6 g,可知燃烧生成水、二氧化碳分别是2.7g和6.6 g,根据元素守恒计算;羟基有1个没成对电子;根据M 的核磁共振氢谱图,可知M有4组峰,比值为1:1:1:3;
解析:(1)根据相同条件下密度比等于摩尔质量之比,其密度是相同条件下H2的45倍,所以摩尔质量是氢气的2倍,M的摩尔质量是90g/mol;(2) 燃烧生成水、二氧化碳分别是2.7g和6.6 g,氢元素的质量为0.3g、碳元素的质量为1.8g,所以4.5g M中元素的质量为2.4g,C、H、O的物质的量比为1:2:1,摩尔质量是90g/mol,所以分子式为C3H6O3;(2)羟基的电子式![]() ;(4)M中含有羟基、羧基,根据M 的核磁共振氢谱图,可知M有4组峰,即有4种等效氢,比值为1:1:1:3;(5)综上所述,M 的结构简式为
;(4)M中含有羟基、羧基,根据M 的核磁共振氢谱图,可知M有4组峰,即有4种等效氢,比值为1:1:1:3;(5)综上所述,M 的结构简式为![]() ;
;

【题目】氮的化合物在生产生活中广泛存在。
(1)①氯胺(NH2Cl)的电子式为________。可通过反应NH3(g)+Cl2(g)=NH2Cl(g)+HCl(g)制备氯胺,已知部分化学键的键能如右表所示(假定不同物质中同种化学键的键能一样),则上述反应的ΔH=_________。
化学键 | 键能/(kJ·mol-1) |
N-H | 391.3 |
Cl-Cl | 243.0 |
N-Cl | 191.2 |
H-Cl | 431.8 |
②NH2Cl与水反应生成强氧化性的物质,可作长效缓释消毒剂,该反应的化学方程式为________。
(2)用焦炭还原NO的反应为:2NO(g)+C(s)![]() N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
t/min | 0 | 40 | 80 | 120 | 160 |
n(NO)(甲容器)/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
n(NO)(乙容器)/mol | 1.00 | 0.80 | 0.65 | 0.53 | 0.45 |
n(NO)(丙容器)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
①该反应为____________(填“放热”或“吸热”)反应。
②乙容器在200min达到平衡状态,则0~200min内用NO的浓度变化表示的平均反应速率v(NO)=_________。
(3)用焦炭还原NO2的反应为:2NO2(g)+2C(s) ![]() N2(g)+2CO2(g),在恒温条件下,1molNO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),在恒温条件下,1molNO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
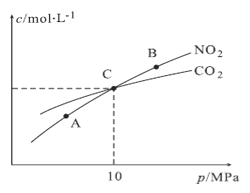
①A、B两点的浓度平衡常数关系:Kc(A)_____Kc(B)(填“<”或“>”或“=”)。
②A、B、C三点中NO2的转化率最高的是______(填“A”或“B”或“C”)点。
③计算C点时该反应的压强平衡常数Kp(C)=______(Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。