题目内容
18.下列实验装置能达到实验目的,且实验装置图无明显错误的是(夹持仪器未画出)( )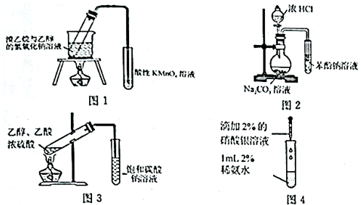
| A. | 图1可表示溴乙烷法制乙烯并验证乙烯 | |
| B. | 图2装置可证明酸性:盐酸>碳酸>苯酚 | |
| C. | 图3用于实验室制备乙酸乙酯 | |
| D. | 图4用于配制银氨溶液 |
分析 A.乙醇易挥发,乙醇、乙烯均能使高锰酸钾褪色;
B.盐酸易挥发,盐酸可与苯酚钠反应;
C.乙醇、乙酸在浓硫酸作用下发生酯化反应生成乙酸乙酯,饱和碳酸钠可吸收乙醇、乙酸,与碳酸钠分层;
D.向硝酸银溶液中滴加氨水,生成沉淀时继续滴加氨水,沉淀恰好溶解即为银氨溶液.
解答 解:A.乙醇易挥发,乙醇、乙烯均能使高锰酸钾褪色,没有排除乙醇的干扰不能检验乙烯,故A错误;
B.盐酸易挥发,盐酸可与苯酚钠反应,则图中装置不能比较碳酸、苯酚的酸性,故B错误;
C.乙醇、乙酸在浓硫酸作用下发生酯化反应生成乙酸乙酯,饱和碳酸钠可吸收乙醇、乙酸,与碳酸钠分层,图中装置可制备乙酸乙酯,故C正确;
D.向硝酸银溶液中滴加氨水,生成沉淀时继续滴加氨水,沉淀恰好溶解即为银氨溶液,则图中试剂的加入顺序不合理,应向硝酸银溶液中滴氨水,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,涉及有机物的结构与性质、酸性比较、物质制备实验等,把握反应原理、实验细节及实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
相关题目
8.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 100 mL 0.1 mol•L-1 Na2SO4溶液中,粒子总数是0.03NA | |
| B. | 常温常压下,32 g O2-中所含电子的数目为17NA | |
| C. | 1 mol Al3+完全水解生成氢氧化铝胶体粒子的数目为NA | |
| D. | 标准状况下,分子数为NA的N2、C2H4混合气体的质量无法确定 |
9.下列反应的离子方程式正确的是( )
| A. | 次氯酸钙溶液中通入过量二氧化碳 Ca2++2ClO-+H2O+CO2═CaCO3↓+2HClO | |
| B. | 硫酸亚铁溶液中加过氧化氢溶液 Fe2++2H2O2+4H+═Fe3++4H2O | |
| C. | Fe2(SO4)3的酸性溶液中通入足量硫化氢 Fe3++H2S═Fe2++S↓+2H+ | |
| D. | 氯化亚铁溶液中加入稀硝酸 3Fe2++4H++NO3-═3Fe3++2H2O+NO↑ |
6.下列离子方程式书写正确的是( )
| A. | 稀硫酸滴在铜片上:Cu+2H+═Cu2++H2↑ | |
| B. | 氢氧化镁与硫酸溶液反应:OH-+H+═H2O | |
| C. | 氢氧化钡溶液与稀硫酸的反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | 将金属Cu加入FeCl3溶液中:2Fe3++Cu═2Fe2++Cu2+ |
13.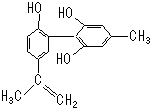 增大我国支持“人文奥运”的一个重要体现是:坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )
增大我国支持“人文奥运”的一个重要体现是:坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )
 增大我国支持“人文奥运”的一个重要体现是:坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )
增大我国支持“人文奥运”的一个重要体现是:坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )| A. | 遇FeCl3溶液显紫色,因为该物质与苯酚属于同系物 | |
| B. | 1 mol该物质与浓溴水和H2反应最多消耗Br2和H2分别为4 mol、7 mol | |
| C. | 滴入KMnO4(H+)溶液,观察紫色褪去,能证明结构中存在碳碳双键 | |
| D. | 该分子中的所有碳原子不可能都共平面 |
3.下列关于化石燃料的说法错误的是( )
| A. | 石油中含有C5~C11的烷烃,可以通过石油的分馏得到汽油 | |
| B. | 含C18以上烷烃的重油经过催化裂化可以得到汽油 | |
| C. | 煤是由有机化合物和无机物组成的复杂的混合物 | |
| D. | 煤中含有苯和甲苯,可以用分馏的方法把它们从煤中分离出来 |
10.在CH3COOH?CH3COO-+H+的电离平衡中,要使电离平衡右移且氢离子浓度增大,应采取的措施是( )
| A. | 加入NaOH | B. | 加入盐酸 | C. | 加水 | D. | 升高温度 |
8.下列说法正确的是( )
| A. | 原子间的相互作用称为化学键 | |
| B. | 破坏旧化学键,需要放出一定的能量 | |
| C. | 在化学反应中不仅有物质的变化,还伴随着能量的变化 | |
| D. | 人们利用化学反应,只是为了制取所需要的物质 |
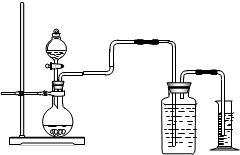 某化学兴趣小组用如图装置进行氢气的制备:试回答下列问题:
某化学兴趣小组用如图装置进行氢气的制备:试回答下列问题: