题目内容
I.有下列物质:①冰醋酸 ②金刚石 ③碳化硅 ④干冰 ⑤过氧化氢 ⑥白磷
根据要求用序号填空.
(1)属于原子晶体的化合物是
II.在①H2O、②H2S、③BF3、④CS2、⑤CCl4、⑥N2、⑦SO2、⑧C2H2分子中:
(1)全部以非极性键结合的非极性分子是
(2)全部以极性键相结合,具有直线型结构的非极性分子是
(3)中心原子为sp3杂化的极性分子
(4)中心原子为sp2杂化的极性分子
(5)既有极性键又有非极性键的非极性分子
根据要求用序号填空.
(1)属于原子晶体的化合物是
③
③
. (2)由极性分子构成的晶体是①⑤
①⑤
,属于分子晶体的单质是⑥
⑥
.(3)在一定条件下.受热熔化需克服共价键的是②③
②③
.II.在①H2O、②H2S、③BF3、④CS2、⑤CCl4、⑥N2、⑦SO2、⑧C2H2分子中:
(1)全部以非极性键结合的非极性分子是
⑥
⑥
.(填序号 下同)(2)全部以极性键相结合,具有直线型结构的非极性分子是
④
④
.(3)中心原子为sp3杂化的极性分子
①②
①②
.(4)中心原子为sp2杂化的极性分子
⑦
⑦
.(5)既有极性键又有非极性键的非极性分子
⑧
⑧
.分析:I.(1)构成微粒为原子,以共价键结合形成网状结构的晶体为原子晶体;
(2)由极性分子构成的晶体为分子晶体,结构不对称,而分子晶体的构成微粒为分子;
(3)由共价键形成的原子晶体熔化需要克服共价键;
II.(1)同种非金属元素形成非极性键,结构对称的分子为非极性分子;
(2)不同种非金属元素形成极性键,结构对称的分子为非极性分子;
(3)成键数与孤对电子数之和为4的为sp3杂化;
(4)成键数与孤对电子数之和为3的为sp2杂化;
(5)同种非金属元素形成非极性键,不同种非金属元素形成极性键.
(2)由极性分子构成的晶体为分子晶体,结构不对称,而分子晶体的构成微粒为分子;
(3)由共价键形成的原子晶体熔化需要克服共价键;
II.(1)同种非金属元素形成非极性键,结构对称的分子为非极性分子;
(2)不同种非金属元素形成极性键,结构对称的分子为非极性分子;
(3)成键数与孤对电子数之和为4的为sp3杂化;
(4)成键数与孤对电子数之和为3的为sp2杂化;
(5)同种非金属元素形成非极性键,不同种非金属元素形成极性键.
解答:解:I.(1)构成微粒为原子,以共价键结合形成网状结构的晶体为原子晶体,只有②③为原子晶体,且③为化合物,故答案为:③;
(2)给出的物质中,只有①⑤为由极性分子构成的晶体,而⑥属于分子晶体,但属于单质,故答案为:①⑤;⑥;
(3)由共价键形成的原子晶体熔化需要克服共价键,则给出的物质中②③符合,故答案为:②③;
II.在①H2O、②H2S、③BF3、④CS2、⑤CCl4、⑥N2、⑦SO2、⑧C2H2分子中,
(1)全部以非极性键结合的非极性分子是⑥,故答案为:⑥;
(2)全部以极性键相结合,具有直线型结构的非极性分子是④,故答案为:④;
(3)中心原子为sp3杂化的极性分子是①②,故答案为:①②;
(4)中心原子为sp2杂化的极性分子是⑦,故答案为:⑦;
(5)既有极性键又有非极性键的非极性分子是⑧,故答案为:⑧.
(2)给出的物质中,只有①⑤为由极性分子构成的晶体,而⑥属于分子晶体,但属于单质,故答案为:①⑤;⑥;
(3)由共价键形成的原子晶体熔化需要克服共价键,则给出的物质中②③符合,故答案为:②③;
II.在①H2O、②H2S、③BF3、④CS2、⑤CCl4、⑥N2、⑦SO2、⑧C2H2分子中,
(1)全部以非极性键结合的非极性分子是⑥,故答案为:⑥;
(2)全部以极性键相结合,具有直线型结构的非极性分子是④,故答案为:④;
(3)中心原子为sp3杂化的极性分子是①②,故答案为:①②;
(4)中心原子为sp2杂化的极性分子是⑦,故答案为:⑦;
(5)既有极性键又有非极性键的非极性分子是⑧,故答案为:⑧.
点评:本题考查化学键及晶体类型,明确判断化学键的一般规律、晶体的构成微粒及分子的极性即可解答,综合性较强,涉及知识点较多,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 是由于 。
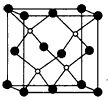
是由于 。 原子在基态时,其价电子轨道表示式为: 。GaAs的晶胞结构如图(As位于顶点和面心),晶胞中与As原子等距离且最近的Ga原子有 个。
原子在基态时,其价电子轨道表示式为: 。GaAs的晶胞结构如图(As位于顶点和面心),晶胞中与As原子等距离且最近的Ga原子有 个。