题目内容
已知下列两个热化学方程式:H2(g)+ ![]() O2(g)
O2(g)![]() H2O(l) ΔH=-285.8 kJ·mol-1
H2O(l) ΔH=-285.8 kJ·mol-1
C3H8(g)+5O2(g)![]() 3CO2(g)+4H2O(l) ΔH=-2 220.0 kJ·mol-1
3CO2(g)+4H2O(l) ΔH=-2 220.0 kJ·mol-1
实验测得氢气和丙烷的混合气体共5 mol,完全燃烧时放热3 847 kJ,则混合气体中氢气和丙烷的体积比是__________;两者放出的热量之比约为__________。
A.1∶3 B.3∶1 C.1∶4 D.5∶13
解析:该题可采用以下两种方法巧解。
方法一:十字交叉法
![]()
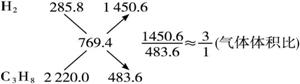
![]()
方法二:估算排除法
因C3H8的燃烧热为2 220.0 kJ·mol-1,而两者燃烧共放热3 874 kJ,故H2和C3H8的体积比一定大于1∶1,而四个选项中唯有B选项3∶1>1∶1符合题意。
两者放出的热量之比也只需列出解法一中的计算式,再估算并对照选项便可选定D选项为答案。
答案:B D

练习册系列答案
相关题目