题目内容
氯气是一种重要的化工原料,自来水的消毒、农药的生产、药物的合成等都需要用氯气。
I.工业上通常采用电解法制氯气:观察右图,回答:

(1)若饱和食盐水中通电后b侧产生的气体通入NaOH溶液中所发生的反应的离子方程式为 。
(2)电解反应的化学方程式为 。
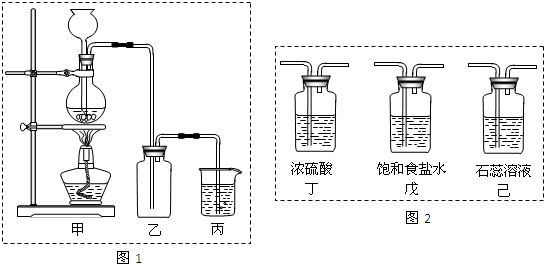
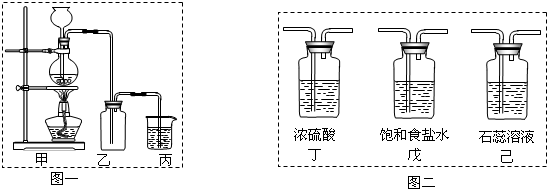
II.某学生设计如右图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应),回答下列问题:

(1)在A装置中用固体二氧化锰与浓盐酸在加热条件下制取氯气,反应化学方程式为 ▲ ,若在标准状态下收集到22.4升的氯气,则被氧化的HCl的物质的量是 ▲ 。
(2)漂白粉将在U形管中产生,其化学方程式是 ▲ 。
(3)C装置的作用是 ▲ 。
(4)此实验所得漂白粉的有效成分偏低,该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应。
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是 ▲ 。
②试判断另一个副反应(用化学方程式表示) ▲ 。为避免此副反应的发生,可将装置作何改进 ▲ 。
(5)家庭中使用漂白粉时,为了增强漂白能力,可加入少量的物质是 ▲ 。
A.食盐 B.食醋 C.烧碱 D.纯碱
I. (1)Cl2+2OH-= Cl –+ClO-+ H2O(2)2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑(注明反应条件:通电,若无酌情)
2NaOH+H2↑+Cl2↑(注明反应条件:通电,若无酌情)
II. (1)MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O , 2mol
MnCl2+Cl2↑+2H2O , 2mol
(2) 2Cl2+2Ca(OH)2 =CaCl2 + Ca(ClO)2 +2H2O
(3) 吸收未反应完的氯气,防止污染空气
(4) ①冷却B装置
②2HCl+Ca(OH)2 =CaCl2 +2H2O 在A与B之间连接一个装有饱和氯化钠溶液的洗气瓶。
(5) B