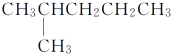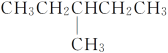题目内容
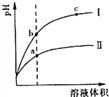
【题目】已知H2R为二元弱酸,25℃用Na2R溶液吸收H2R,吸收液的pH与![]() 的关系如下图所示:
的关系如下图所示:

下列说法中正确的是
A. NaHR溶液中:c(Na+)<c(HR-)+2c(R2-)
B. 25℃Ka1(H2R)的值为10-7.2
C. Na2R溶液中:c(Na+>c(R2-)>c(HR-)>c(OH-)
D. 当吸收液呈中性时:c(R2-)>c(HR-)
【答案】A
【解析】A.根据图像中吸收液的pH随![]() 变化的关系可知,随着HR-的浓度的增大,溶液酸性增强,说明NaHR溶液显示酸性,即:c(H+)>c(OH-),根据电荷守恒,c(Na+)+ c(H+)=c(HR-)+2c(R2-)+ c(OH-),因此c(Na+)<c(HR-)+2c(R2-),故A正确;B.根据图像,当
变化的关系可知,随着HR-的浓度的增大,溶液酸性增强,说明NaHR溶液显示酸性,即:c(H+)>c(OH-),根据电荷守恒,c(Na+)+ c(H+)=c(HR-)+2c(R2-)+ c(OH-),因此c(Na+)<c(HR-)+2c(R2-),故A正确;B.根据图像,当![]() =1时,pH=7.2,则25℃,Ka2(H2R)=
=1时,pH=7.2,则25℃,Ka2(H2R)=  = 10-7.2,则Ka1(H2R)>10-7.2,故B错误;C.Na2R溶液中,R2-在溶液中水解程度较小,则c(R2-)>c(HR-),由于氢氧根离子来自R2-的水解和水的电离,则c(OH-)>c(HR-),溶液中离子浓度大小为:c(Na+)>c(R2-)>c(OH-)>c(HR-)>c(H+),故C错误;D.根据图像,吸收液呈中性时,
= 10-7.2,则Ka1(H2R)>10-7.2,故B错误;C.Na2R溶液中,R2-在溶液中水解程度较小,则c(R2-)>c(HR-),由于氢氧根离子来自R2-的水解和水的电离,则c(OH-)>c(HR-),溶液中离子浓度大小为:c(Na+)>c(R2-)>c(OH-)>c(HR-)>c(H+),故C错误;D.根据图像,吸收液呈中性时,![]() >1,即c(R2-)<c(HR-),故D错误;故选A。
>1,即c(R2-)<c(HR-),故D错误;故选A。

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案【题目】某学习小组研究影响锌与稀硫酸反应速率的外界条件,设计实验的数据如下:
实验序号 | 锌的质量/g | 锌的状态 | c(H2SO4)/mol·L-1 | V(H2SO4)/mL | 反应前溶液的温度/℃ | 其他试剂 |
1 | 0.65 | 粒状 | 0.5 | 50 | 20 | 无 |
2 | 0.65 | 粉末 | 0.5 | 50 | 20 | 无 |
3 | 0.65 | 粒状 | 0.5 | 50 | 20 | 2滴CuSO4溶液 |
4 | 0.65 | 粉末 | 0.8 | 50 | 20 | 无 |
5 | 0.65 | 粉末 | 0.8 | 50 | 35 | 2滴CuSO4溶液 |
(1)在此5组实验中,判断锌和稀硫酸反应速率大小,最简单的方法可通过测定 进行判断,其速率最快的是 (填实验序号)。
(2)实验1和2表明 对反应速率有影响;实验1和3表明 对反应速率有影响。
(3)进行实验2时,小组同学根据实验过程绘制的氢气体积(标准状况下)与时间的关系如图所示。
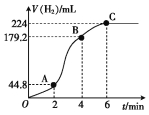
①在OA、AB、BC三段中反应速率最快的是 ,其原因是 。
②2~4 min内以硫酸的浓度变化表示的反应速率(假设溶液的体积不变)v(H2SO4)= mol·L-1·min-1。
【题目】乙苯( )是重要的化工原料,工业上利用乙苯可以制备苯乙烯和β-氯苯乙烷:
)是重要的化工原料,工业上利用乙苯可以制备苯乙烯和β-氯苯乙烷:
乙苯脱氢制苯乙烯:
![]() △H1=akJ/mol
△H1=akJ/mol
乙苯氯化制β-氯苯乙烷:
![]() △H2=bkJ/mol
△H2=bkJ/mol
回答下列问题:
(1)利用下表提供的数据计算a=_____。乙苯脱氢制苯乙烯的反应在_____(填“高温”或“低温”)有利于其自发进行。
化学键 | C-H | C-C | H-H | C=C |
键能/kJ/mol | 412 | 348 | 436 | 612 |
(2)已知
![]() +HCl(g)
+HCl(g)![]()
![]() △H=-54kJ/mol
△H=-54kJ/mol
H2(g)+Cl2(g)=2HCl(g) △H=-185kJ/mol 则b=______________。
(3)T℃,将nmol乙苯加入到体积为V L的恒容容器中,发生脱氢反应,容器内压强随时间变化如下表所示:
时间/min | 0 | 10 | 20 | 30 | 40 |
压强/×100 kPa | 1.0 | 1.2 | 1.3 | 1.4 | 1.4 |
平衡时容器内气体的总物质的量为______,乙苯的转化率为______%。
(4)工业由乙苯脱氢制苯乙烯实际上是在恒压密闭容器中进行的。将m mol乙苯通入某恒压密闭容器中(反应过程中维持压强为p),乙苯的平衡转化率随温度变化如右图所示:
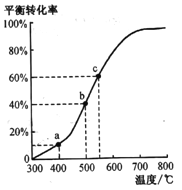
①在a点所示的条件下,向该容器中通入25L水蒸气,则乙苯的转化率______(填“变大”“变小”或不变),生成苯乙烯的速率________(填“变大”“变小”或不变)。
②b点气体总体积______(填“<”“>”或“=”)c 点气体总体积。
③c点平衡常数Kp=_______(用平衡分压代替平衡浓度,平衡分压=物质的量分数×总压)。