题目内容
【题目】设NA代表阿伏加德罗常数,下列说法正确的是( )
A.5.6g铁与足量盐酸反应转移的电子数为0.3NA
B.100mL2.0mol/L的氢氧化钠溶液与氢氧化钡溶液中氢氧根离子均为0.2NA
C.标准状况下,22.4L氦气与11.2L氯气所含原子数均为NA
D.16g18O2与16g16O3所含的中子数均是8NA
【答案】C
【解析】
A.5.6g铁的物质的量为0.1mol,铁与盐酸反应生成氯化亚铁和氢气,铁由0价升高为+2价,转移的电子数为![]() ,故A错误;
,故A错误;
B. 氢氧化钠为强电解质完全电离,100mL2mol/L的氢氧化钠中氢氧根离子数目为![]() ,氢氧化钡为二元强碱,100mL2mol/L的氢氧化钡中氢氧根离子数目为
,氢氧化钡为二元强碱,100mL2mol/L的氢氧化钡中氢氧根离子数目为![]() ,故B错误;
,故B错误;
C. 标准状况下,22.4L氦气为1mol,所含原子数为![]() ,11.2L氯气为0.5mol,所含原子数为
,11.2L氯气为0.5mol,所含原子数为![]() ,故C正确;
,故C正确;
D.16g![]() 的物质的量是
的物质的量是![]() ,所含中子数为:
,所含中子数为:![]() , 16g
, 16g![]() 的物质的量为
的物质的量为![]() ,所含的中子数为:
,所含的中子数为:![]() ,故D错误;
,故D错误;
故答案选C。

 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案【题目】下表是元素周期表的一部分,请回答有关问题:
主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
二 | ① | ② | ||||||
三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
四 | ⑨ | ⑩ |
(1)表中化学性质最不活泼的元素是______。(用元素符号表示)
(2)②③④三种元素的原子半径从大到小的顺序是______(用元素符号表示)
(3)用电子式表示③与⑦形成化合物的过程_______________________。
(4)在①~⑧元素中,元素的最高价氧化物对应的水化物中碱性最强的___。(填化学式)
(5)在⑦与⑩的单质中,化学性质较活泼的是_____。(填化学式)
【题目】某研究小组利用如图所示的装置,进行CO还原Fe2O3的实验(固定装置略)。
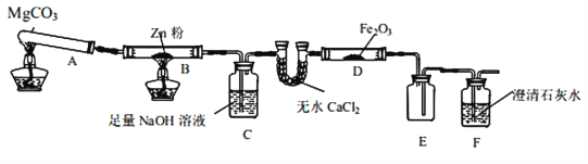
(1)装置B中发生的化学方程式________________。装置C的作用是__________________________
(2)用酒精喷灯对装置D加热,得到灰黑色粉末用黑色粉末进行以下实验:
步骤 | 操作 | 现象 |
1 | 取灰黑色粉末加入稀硫酸 | 溶解,有气泡 |
2 | 取步骤1中溶液,滴加NaOH溶液后,在空气中,搅拌放置 | 白色沉淀最终变为红褐色 |
3 | 取步骤1中溶液,滴加KSCN溶液 | 无现象 |
4 | 向步骤3溶液中滴加新制氯水至过量 | 先变红,后褪色 |
①得到的灰黑色粉末是________________(填写化学式)。
②步骤2中“白色沉淀最终变为红褐色”的化学反应方程式为_________________。
③步骤4中,溶液变红的原因为_____________________________________________________________;溶液褪色可能的原因______________________________________;验证上述原因的实验操作方法为____________。
(3)上述装置,从实验安全考虑,需要采取的改进措施是________。