��Ŀ����
����Ŀ��Ԫ�ظ�(Cr)����Ȼ����Ҫ�ԣ�3�ۺͣ�6�۴��ڡ��ش��������⣺
(1)��6�۵�Cr������ϸ������������岻��������Na2SO3��Cr2O72����ԭΪCr3������Ӧ�����ӷ���ʽΪ____________________��
(2)���ø�����(FeO��Cr2O3)ұ����ȡ�������Ĺ���������ͼ��ʾ��
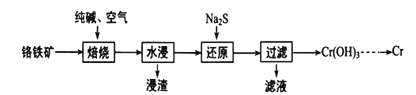
��Ϊ�ӿ챺�����ʺ����ԭ�ϵ������ʣ��ɲ�ȡ�Ĵ�ʩ��_________(дһ��)��
����ˮ������Ҫ��ý���Һ�IJ�����_______������Һ����Ҫ�ɷ�ΪNa2CrO4��������Һ���м����ữ���Ȼ�����Һ�а�ɫ�������ɣ�������ԭ�������з�����Ӧ�����ӷ���ʽΪ______��
�ۼ���Cr(OH)3�ɵõ�Cr2O3���ӹ�ҵ�ɱ��Ƕȿ��ǣ���Cr2O3��ȡ����Cr��ұ��������_________��
���𰸡�3SO32-+8H++Cr2O72��=2Cr3++3SO42-+4H2O ����������� ���� 3S2-+20H2O+8Cr2O72��=8Cr(OH)3��+3SO42- +16OH- �����£���CO��ԭ���Ȼ�ԭ��
��������
(1)��Ӧ�и�Ԫ�ػ��ϼ۴ӣ�6�۽�Ϊ+3�ۣ���Ԫ�ش�+4�����ߵ�+6�ۣ����ݵ�ʧ�����غ㣬ԭ�Ӹ����غ㣬���ӷ�Ӧ����ʽΪ3SO32-+8H++Cr2O72��=2Cr3++3SO42-+4H2O��
(2)��Ӱ�컯ѧ��Ӧ���ʵ����������Ҫ�����ʵı������С�������Խ��Ӧ����Խ�죬��Ϊ�ӿ챺�����ʺ����ԭ�ϵ������ʣ��ɲ�ȡ�Ĵ�ʩ�Ƿ��������
����ˮ����Ҫ��ý���Һ��Ҫ���˳���������ȡ�IJ����ǹ��ˣ�����Һ����Ҫ�ɷ�ΪNa2CrO4��������Һ���м����ữ���Ȼ�����Һ�а�ɫ�������ɣ�˵�������Na2S��������SO42-��CrԪ����+6�۽�Ϊ+3�ۣ�SԪ����-2������+6�ۣ�����ԭ���غ�͵�ʧ�����غ㣬�õ���ӦΪ3S2-+20H2O+8Cr2O72��=8Cr(OH)3��+3SO42- +16OH-��
�۴ӹ�ҵ�ɱ��Ƕȿ��ǣ���Cr2O3��ȡ����Cr�����Բ�ȡCO���»�ԭCr2O3 (�Ȼ�ԭ��)��

 �߽�������ϵ�д�
�߽�������ϵ�д�����Ŀ��һ���¶��£���3�������Ϊ1.0 L�ĺ����ܱ������з�Ӧ2H2(g)��CO(g)![]() CH3OH(g)�ﵽƽ�⣬����˵����ȷ����( )
CH3OH(g)�ﵽƽ�⣬����˵����ȷ����( )
���� | �¶�/K | ���ʵ���ʼŨ��/mol��L��1 | ���ʵ�ƽ��Ũ��/mol��L��1 | ||
c(H2) | c(CO) | c(CH3OH) | c(CH3OH) | ||
�� | 400 | 0.20 | 0.10 | 0 | 0.080 |
�� | 400 | 0.40 | 0.20 | 0 | |
�� | 500 | 0.20 | 0.10 | 0 | 0.025 |
A. �÷�Ӧ������Ӧ����
B. �ﵽƽ��ʱ���������з�Ӧ��ת���ʱ��������еĴ�
C. �ﵽƽ��ʱ����������c(H2)������������c(H2)������
D. �ﵽƽ��ʱ���������е�����Ӧ���ʱ��������еĴ�
����Ŀ������ʵ���У���Ӧ�������Լ����۶���ȷ����
ѡ�� | ʵ�� | ���� | ���� |
A | ��Ƶε�����Ƭ�� | ����Ƭ���� | ��������Ԫ�ر��� |
B | ���Թ���CH4��Cl2����1��1��ϣ����ڹ����� | �Թ���������ɫ��dz���Թܱڳ�����״Һ�Σ������а��� | ���������£�CH4��Cl2�����˻�ѧ�仯 |
C | ��20%������Һ�м�������ϡ���ᣬ���ȣ��ټ�������������ͭ���ټ��������� | ���������� | ����δ����ˮ�� |
D | С�鼦Ƥ�ϵμ�3��5��Ũ���� | ��Ƥ�ɰױ�� | �����ʶ��ܷ�����ɫ�仯 |
A.AB.BC.CD.D