题目内容
【题目】软锰矿主要含有MnO2(约70%)、SiO2、Al2O3,闪锌矿主要含有ZnS(约80%)、FeS、CuS、SiO2。为了高效利用这两种矿石,科研人员开发了综合利用这两种资源的同槽酸浸工艺,主要流程如下图所示,回答下列问题:
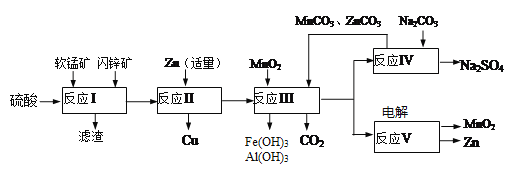
(1)反应Ⅰ所得滤液中含有Mn2+、Zn2+、Cu2+、Fe3+、Al3+等金属阴离子,所得滤液中含有S和______。为了提高硫酸“酸浸”时的浸出速率,可进行的操作是(至少两条):_________。
(2)若反成Ⅱ加入的锌过量,还会进一步发生反应的离子方程式方为_________。
(3)反应Ⅲ中加入MnO2的作用是(离子方程式表示)________;反应Ⅲ中加入MnCO3、ZnCO3的作用是________________。
(4)反应Ⅴ的电解总反应为:MnSO4+ZnSO4+2H2O![]() MnO2+Zn+2H2SO4,写出阳极的电极反应式________________。
MnO2+Zn+2H2SO4,写出阳极的电极反应式________________。
(5)MnO2和Zn可按等物质的量之比生产锌-锰干电池,则从生产MnO2和Zn的角度计算,所用软锰矿和闪铲矿的质量比大约是______。(保留小数点后两位)
【答案】 SiO2 提高温度、适量增加硫酸浓度、将矿石粉碎或搅拌或借助鼓风机等 Zn+Fe2+=Zn2++Fe 4H++MnO2+2Fe2+=Mn2++2Fe3++2H2O 调节pH,使Fe3+和Al3+沉淀,且不引入杂质 Mn2+-2e-+2H2O=MnO2+4H+ 1.03
【解析】(1)因为软锰矿主要含有MnO2(约70%)、SiO2、Al2O3,闪锌矿主要含有ZnS(约80%)、FeS、CuS、SiO2,反应Ⅰ中加H2SO4所得滤液中含有Mn2+、Zn2+、Cu2+、Fe3+、Al3+等金属阳离子, SiO2不能和H2SO4反应,所得滤液中含有S和SiO2。为了提高硫酸“酸浸”时的浸出速率,可提高温度、适量增加硫酸浓度、将矿石粉碎或搅拌或借助鼓风机等方法来加快反应速率。答案:SiO2 提高温度、适量增加硫酸浓度、将矿石粉碎或搅拌或借助鼓风机等。
(2)若反成Ⅱ加入的锌过量,还会与Fe2+发生反应,反应的离子方程式方为Zn+Fe2+=Zn2++Fe.
(3)反应Ⅲ中加入的MnO2是氧化剂,可以把Fe2+氧化成Fe3+,离子方程式为4H++MnO2+2Fe2+=Mn2++2Fe3++2H2O;反应Ⅲ中加入的MnCO3、ZnCO3可以和酸反应,所以可用来调节溶液的酸碱性,使Fe3+和Al3+沉淀,且不引入杂质。
(4)反应Ⅴ的电解总反应为:MnSO4+ZnSO4+2H2O![]() MnO2+Zn+2H2SO4,阳极发生氧化反应失电子,其电极反应式Mn2+-2e-+2H2O=MnO2+4H+。
MnO2+Zn+2H2SO4,阳极发生氧化反应失电子,其电极反应式Mn2+-2e-+2H2O=MnO2+4H+。
(5))据反应MnSO4+ZnSO4+2H2O=MnO2+Zn+2H2SO4可知MnO2、Zn的物质的量之比为1:1,故可设软锰矿、闪锌矿的质量分别为x、y,得0.7x/87:0.8y/97=1:1,故x:y=1.03.。所用软锰矿和闪铲矿的质量比大约是1.03。