题目内容
O2、SO2、SO3三者的质量比为2:4:5时,它们的物质的量之比为( )
| A、2:4:5 | B、1:2:3 | C、1:1:1 | D、2:2:3 |
分析:根据n=
可知物质的物质的量,再计算它们的物质的量之比.
| m |
| M |
解答:解:O2、SO2、SO3三者的质量比为2:4:5,
O2、SO2、SO3三者的摩尔质量分别为32g/mol、64g/mol、80g/mol,
由n=
可知,
它们的物质的量之比为
:
:
=1:1:1,
故选C.
O2、SO2、SO3三者的摩尔质量分别为32g/mol、64g/mol、80g/mol,
由n=
| m |
| M |
它们的物质的量之比为
| 2 |
| 32 |
| 4 |
| 64 |
| 5 |
| 80 |
故选C.
点评:本题考查物质的量的有关计算,明确质量、物质的量、摩尔质量的关系即可解答,难度不大.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目

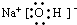
 H++HO2ˉ
H++HO2ˉ