题目内容
【题目】在调节好pH和![]() 浓度的废水中加
浓度的废水中加![]() ,能氧化降解污染物。现用该方法降解污染物
,能氧化降解污染物。现用该方法降解污染物![]() ,控制
,控制![]() 、
、![]() 和
和![]() 的初始浓度相同,设计如下对比实验探究温度、pH对该降解反应速率的影响,测得
的初始浓度相同,设计如下对比实验探究温度、pH对该降解反应速率的影响,测得![]() 的浓度随时间变化的关系如下图。
的浓度随时间变化的关系如下图。

下列结论或推断不正确的是
A.实验①、②表明适当升高温度,降解反应速率增大
B.根据反应原理推断,温度过高,反而会使降解速率变慢
C.313K、![]() 时,在
时,在![]() 内,
内,![]() 的分解平均速率约为
的分解平均速率约为![]() mol/(L·s)
mol/(L·s)
D.室温下,实验过程中取样分析浓度可以采用迅速加碱调节溶液pH的方法
【答案】C
【解析】
A.实验![]() 、
、![]() 的温度不同,根据图示,表明适当升高温度,降解反应速率增大,故A正确;
的温度不同,根据图示,表明适当升高温度,降解反应速率增大,故A正确;
B. 温度过高,![]() 分解速率加快,所以会使
分解速率加快,所以会使![]() 降解速率变慢,故B正确;
降解速率变慢,故B正确;
C.根据图象可知,曲线![]() 中在
中在![]() 内,
内,![]() 浓度由
浓度由![]() 下降为
下降为![]() ,则
,则![]() 内的平均反应速率为:
内的平均反应速率为:![]()
![]() mol/(L·s) ,故C错误;
mol/(L·s) ,故C错误;
![]() 室温下,实验
室温下,实验![]() 、
、![]() 表明在实验过程中取样分析浓度可以采用迅速加碱调节溶液pH的方法,故D正确。
表明在实验过程中取样分析浓度可以采用迅速加碱调节溶液pH的方法,故D正确。
故选C。

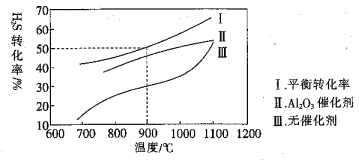
【题目】合成氨工业涉及固体燃料的气化,需要研究CO2与CO之间的转化。为了弄清其规律,让一定量的CO2与足量碳在体积可变的密闭容器中反应:C(s)+CO2(g) ![]() 2CO(g) H,测得压强、温度对CO、CO2的平衡组成的影响如图所示,回答下列问题:
2CO(g) H,测得压强、温度对CO、CO2的平衡组成的影响如图所示,回答下列问题:

(1)p1、p2、p3的大小关系是________,图中a、b、c三点对应的平衡常数大小关系是______________________。
(2)一定条件下,在CO2与足量碳反应所得平衡体系中加入H2和适当催化剂,有下列反应发生:反应1:CO(g)+3H2(g) ![]() CH4(g)+H2O(g) H1= a kJ/mol
CH4(g)+H2O(g) H1= a kJ/mol
反应2:CO(g)+H2O(g) ![]() CO2(g)+H2(g) H2= b kJ/mol
CO2(g)+H2(g) H2= b kJ/mol
① 则二氧化碳与氢气反应转化为甲烷和水蒸气的热化学方程式是____________。
② 已知298 K时相关化学键键能数据为:
化学键 | H—H | O—H | C—H |
|
E/(kJ·mol-1) | 436 | 465 | 413 | 1076 |
则根据键能计算,H1=________________。反应1自发进行的条件是___________。(填“较高温度”、“较低温度”、“任意温度”)
(3)一定条件下,CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ΔH3,向固定容积为1 L的密闭容器中充入2 mol CO2和6 mol H2,一段时间后达到平衡状态,测得CH3OH(g)的物质的量为1mol,则此条件下该反应的化学平衡常数K =_________(用分数表示);若开始时充入2 mol CH3OH(g) 和2 mol H2O(g)达到相同平衡状态时,CH3OH的转化率为_______;若平衡后再充入4 mol的N2,则c(CO2)和原平衡比较是_________。(填“增大”、“减小”、“不变”)
CH3OH(g)+H2O(g) ΔH3,向固定容积为1 L的密闭容器中充入2 mol CO2和6 mol H2,一段时间后达到平衡状态,测得CH3OH(g)的物质的量为1mol,则此条件下该反应的化学平衡常数K =_________(用分数表示);若开始时充入2 mol CH3OH(g) 和2 mol H2O(g)达到相同平衡状态时,CH3OH的转化率为_______;若平衡后再充入4 mol的N2,则c(CO2)和原平衡比较是_________。(填“增大”、“减小”、“不变”)
(4)如图是甲醇燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极。工作一段时间后,断开K,此时A、B两极上产生的气体体积相同。

①甲中负极的电极反式为_______________,丙中C极的电极反应式为___________。
② 乙中A极析出的气体在标准状况下的体积为__________________。
【题目】某研究性学习小组利用H2C2O4溶液和酸性KMnO4溶液之间的反应来探究“外界条件改变对化学反应速率的影响”,实验如下,下列说法错误的是( )
实验 序号 | 实验温度T/K | 参加反应的物质 | 溶液颜色褪至无色时所需时间t/s | ||||
KMnO4溶液(含硫酸) | H2C2O4溶液 | H2O | |||||
V/mL | c/mol·L-1 | V/mL | c/mol·L-1 | V/mL | |||
A | 293 | 4 | 0.02 | 6 | 0.1 | 0 | 6 |
B | 293 | 4 | 0.02 | 4 | 0.1 | V1 | 8 |
C | T1 | 4 | 0.02 | 6 | 0.1 | 0 | 5 |
A.时间t的意义是,从溶液混合到 B.实验C中 C.实验A和B是探究 D.实验A和C是探究温度对反应速率的影响,则![]() 颜色褪去的时间
颜色褪去的时间![]()
![]() 浓度对反应速率的影响,则
浓度对反应速率的影响,则![]()
![]()