题目内容
有A、B、C、D、E五种短周期元素,其原子半径依次增大,B、C同主族,B有两种同素异形体,其中一种可以做漂白剂。C、D、E的最高价氧化物的水化物两两之间均能发生反应。
(1)A、B、C的气态氢化物中最稳定的是: 。(填化学式)
(2)A、B、C的气态氢化物中B的氢化物沸点最高,原因是:
。
(3)B的另一种氢化物能与C的一种含氧酸钠盐的水溶液发生氧化还原反应。写出反应的化学方程式:
。
(4)画出E的原子结构示意图: 。
(5)等物质的量的D、E投入水中充分反应后所得溶液呈碱性,原因是:
。(写离子方程式)
(1) HF 。(填化学式)(2) 水中含有较多的氢键 。
(3) H2O2 + Na2SO3 = H2O + Na2SO4 。(4) 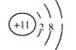 。
。
(5)
AlO2ˉ + 2H2O ![]() Al(OH)3 + OHˉ 。
Al(OH)3 + OHˉ 。
解析:
略

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目





