题目内容
把A、B、C、D四块金属泡在稀H2SO4中,用导线两两相连可以组成各种原电池。若A、B相连时,A为负极;C、D相连,D上有气泡逸出;A、C相连时A极减轻;B、D相连,B为正极。则四种金属的活泼性顺序由大到小排列为
A. A>B>C>D B. A>C>B>D C. A>C>D>B D. B>D>C>A
C
解析试题分析:在原电池中,负极金属的活泼性强于正极金属的活泼性,据此来判断各个原电池中金属的活泼性情况。原电池中,若A、B相连时,A为负极,说明活泼性A>B;C、D相连,D上有气泡逸出,说明D做原电池的正极,C是负极,所以活泼性时C>D;A、C相连时A极减轻,所以A是负极,所以活泼性是A>C;B、D相连,B为正极,所以活泼性是D>B,总上可知金属的活泼性顺序是A>C>D>B,答案选C。
考点:考查利用原电池判断金属活泼性的方法
点评:该题是高考中的常见题型,属于中等难度的试题。主要是考查学生利用原电池原理判断金属性强弱的方法,有利于培养学生的逻辑推理能力和发散思维能力。明确原电池的工作原理、正负极的判断依据是答题的关键,学生不难得分。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列关于元素周期表的说法中,错误的是
| A.元素周期表是元素按原子序数大小排列而成的 |
| B.元素原子的电子层数等于其所在周期的周期序数 |
| C.L层电子为偶数的所有主族元素所在族的序数与该元素原子的L层电子数相等 |
| D.元素周期表是元素周期律的具体表现形式 |
A和B是短周期的两种元素,它们的离子A-和B2+具有相同的核外电子层结构,下列说法中正确的是。
| A.原子序数A>B | B.电子总数A>B |
| C.原子半径A>B | D.离子半径A->B2+ |
铋(Bi)在医药方面有重要应用。 下列关于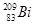 和
和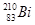 的说法正确的是
的说法正确的是
A.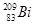 和 和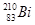 都含有83个中子 都含有83个中子 |
B.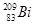 和 和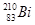 互为同位素 互为同位素 |
C.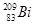 和 和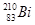 的核外电子数不同 的核外电子数不同 |
D.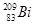 和 和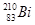 分别含有126和127个质子 分别含有126和127个质子 |
19世纪中叶,俄国化学家门捷列夫
| A.提出了原子分子学说 | B.提出了元素周期律 |
| C.制出了第一张元素周期表 | D.发现了质量守恒定律 |
短周期元素X原子核外的电子处于n个电子层上,最外层电子数为(2n+1),核内质子数为(2n2-1)。有关X的说法中不正确的是 ( )
| A.X能形成化学式为NaXO3的含氧酸钠盐 |
| B.X元素气态氢化物的水溶液呈酸性 |
| C.X原子的最外层电子数和核电荷数不可能为偶数 |
| D.X元素常见单质的化学式为X2 |
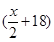 和
和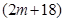
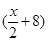 和
和