题目内容
17.X元素天然存在的一个原子中共有质子、中子及电子93个,其中35个粒子不带电,则X元素的该原子的相对原子质量约为( )| A. | 35 | B. | 30 | C. | 64 | D. | 58 |
分析 先根据原子一般是由质子、中子、电子构成的,中子不带电,一个质子带一个单位的正电荷,一个电子带一个单位的负电荷,推算出中子、质子和核外电子的数目,再根据相对原子质量≈质子数+中子数,质子数=电子数进行分析解答.
解答 解:X元素天然存在的一个原子中共有质子、中子及电子93个,其中35个粒子不带电,也就是说有35个中子,质子数和电子数共有93-35=58,又因为原子中质子数=电子数,故质子数为29,
相对原子质量≈质子数+中子数,故其相对原子质量≈29+35=64.
故选:C.
点评 本题难度不大,解题的关键是原子的结构以及构成原子的粒子之间的关系、相对原子质量≈质子数+中子数、原子中核内质子数=核外电子数,难度不大.

练习册系列答案
相关题目
7.人造象牙主要成分的结构是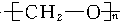 ,它是通过加聚反应制得的,则合成象牙的单体是( )
,它是通过加聚反应制得的,则合成象牙的单体是( )
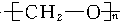 ,它是通过加聚反应制得的,则合成象牙的单体是( )
,它是通过加聚反应制得的,则合成象牙的单体是( )| A. | (CH3)2O | B. | CH3CHO | C. | HCHO | D. | C2H2和H2O |
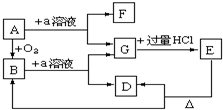 在下列物质的转化关系中,A是一种固体单质,E是一种白色沉淀,F是最轻的气体单质,据此填写下列空白:
在下列物质的转化关系中,A是一种固体单质,E是一种白色沉淀,F是最轻的气体单质,据此填写下列空白: