题目内容
用NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A.0.1mol·L-1稀硫酸100mL中含有硫酸根个数为0.1NA |
| B.1molCH3+(碳正离子)中含有电子数为10NA |
| C.2.4g金属镁与足量的盐酸反应,转移电子数为 2NA |
| D.12.4g白磷中含有磷原子数为0.4NA |
D
考查的知识点为“物质的量及物质的量浓度微粒数目,氧化还原反应中得失电子数目”。
A:H2SO4 2H++SO42- c(SO42-)=0.1mol/L,V=0.1L。
2H++SO42- c(SO42-)=0.1mol/L,V=0.1L。
∴n(SO42-)=0.1mol/L×0.1L=0.01mol,即0.01NA(所以A错);
B:CH3+1mol中含8mol电子,∴电子数应为8NA,(错)
C:Mg+2H+→Mg2++H2↑转移电子
24g 2NA
2.4g 0.2NA(错)
D:考查白磷的化学式P4,1mol P4中有4NA磷原子。12.4g相当于0.1mol P4
∴有0.4 NA磷原子(正确)。
A:H2SO4
 2H++SO42- c(SO42-)=0.1mol/L,V=0.1L。
2H++SO42- c(SO42-)=0.1mol/L,V=0.1L。∴n(SO42-)=0.1mol/L×0.1L=0.01mol,即0.01NA(所以A错);
B:CH3+1mol中含8mol电子,∴电子数应为8NA,(错)
C:Mg+2H+→Mg2++H2↑转移电子
24g 2NA
2.4g 0.2NA(错)
D:考查白磷的化学式P4,1mol P4中有4NA磷原子。12.4g相当于0.1mol P4
∴有0.4 NA磷原子(正确)。

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目

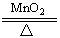 2KCl+3O2↑
2KCl+3O2↑ SO2
SO2 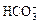 离子数为6.02×1023[
离子数为6.02×1023[ Cu+H2O
Cu+H2O