题目内容
1.制取下列物质,不能直接用乙烯作原料的是( )| A. | CH3CH2Cl | B. | CH2=CHCl | C. | CH3CH2OH | D. | CH2Br-CH2Br |
分析 乙烯含有C=C双键,可与HCl、水、溴等发生加成反应,以此解答该题.
解答 解:A.乙烯与HCl发生加成可生成CH3CH2Cl,可一步得到,故A不选;
B.乙烯不能与Cl2发生取代反应生成CH2=CHCl,故B选;
C.乙烯与水加成加成反应生成CH3CH2OH,故C不选;
D.乙烯与Br2发生加成反应生成CH2Br-CH2Br,故D不选;
故选B.
点评 本题主要考查了乙烯的化学性质,为高频考点,难度不大,注意掌握常见官能团的性质以及反应类型的判断.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
11.下列说法正确的是( )
| A. | 为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH,若pH>7,则H2A是弱酸;若pH<7,则H2A一定是强酸 | |
| B. | 用已知浓度的盐酸滴定未知浓度的氨水,选用最佳指示剂为酚酞 | |
| C. | 为减小洗涤过程中固体的损失,最好选用稀H2SO4代替H2O来洗涤BaSO4沉淀 | |
| D. | 常温下,强酸溶液的pH=a,将溶液的体积稀释到原来的10n倍,则pH=a+n |
12.在某容积一定的密闭容器中,有下列的可逆反应:A(g)+B(g)?xC(g)有图Ⅰ和图Ⅱ所示的反应曲线(T表示温度,P表示压强,C%表示C的体积分数),试判断下列说法中正确的是( )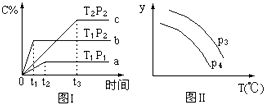

| A. | 正反应为放热,T1>T2 | |
| B. | x=1,P2<P1 | |
| C. | y轴表示混合气体的平均分子量,P3<P4 | |
| D. | y轴表示B的转化率,P3>P4 |
9.下列有关实验或操作的叙述正确的是( )


| A. | 如图甲,检验溴乙烷与NaOH醇溶液共热产生的乙烯 | |
| B. | 如图乙,做喷泉实验时先挤压胶头滴管使水进入烧瓶,后松开止水夹 | |
| C. | 酸碱中和滴定前,滴定管和锥形瓶在用蒸馏水洗涤后均需用待装溶液润洗 | |
| D. | 用托盘天平称取1.06g无水碳酸钠,溶于250mL水,配制0.04 mol•L-1Na2CO3溶液 |
6.下列物质分离过程中涉及共价键断裂的是( )
| A. | 用渗析法除去淀粉胶体中的少量NaCl | |
| B. | 用CCl4萃取碘水中的碘 | |
| C. | 用饱和食盐水洗去Cl2中的少量HCl | |
| D. | 用升华法除去NaCl中混有的少量碘 |
13.下列叙述中正确的是( )
| A. | 22.4L氧气中必然含有6.02×1023个氧分子 | |
| B. | 同温同压下,原子数均为6.02×1023个的氢气和氦气具有相同的体积 | |
| C. | 0.50mol的硫酸钠中含有6.02×1023个钠离子 | |
| D. | 1.0L浓度为1.0mol•L-1的一元酸溶液中含有 6.02×1023个氢离子 |
10.下列各种物质中,既能发生加成反应,又能发生取代反应;既不能与溴水反应,又不能使高锰酸钾溶液褪色的是( )
| A. | 2-甲基-1-丁烯 | B. | 裂化汽油 | C. | 苯 | D. | 邻二甲苯 |
11.被称为“软电池”的纸质电池,采用一个薄层纸片(在其一边镀锌,在其另一边镀二氧化锰)作为传导体.在纸内的离子“流过”水和氧化锌组成的电解液.电池总反应为Zn+2MnO2+H2O═ZnO+2MnO(OH),下列说法正确的是( )
| A. | 该电池的正极为锌 | |
| B. | 该电池反应中二氧化锰起催化剂作用 | |
| C. | 当0.1 mol Zn完全溶解时,流经电解液的电子个数为1.204×1023 | |
| D. | 电池正极反应式为MnO2+e-+H2O═MnO(OH)+OH- |