题目内容
17.用6.02×1023表示阿伏加德罗常数的值,下列说法中正确的是( )| A. | 常温常压下,1.6g臭氧中含有6.02×1022个氧原子 | |
| B. | 标准状况下,2.24L水中含有6.02×1022个水分子 | |
| C. | 2.24L氨气分子中含6.02×1023个电子 | |
| D. | 18gD2O中所含的中子数为10NA |
分析 A、臭氧由氧原子构成;
B、标况下,水为液态;
C、氨气所处的状态不明确;
D、重水的摩尔质量为20g/mol.
解答 解:A、臭氧由氧原子构成,故1.6g臭氧中所含有的氧原子的物质的量为0.1mol,即6.02×1022个,故A正确;
B、标况下,水为液态,不能根据气体摩尔体积来计算,故B错误;
C、氨气所处的状态不明确,不一定是标况,故2.24L氨气的物质的量不一定是0.1mol,故含有的电子数不能计算,故C错误;
D、重水的摩尔质量为20g/mol,故18g中重水的物质的量为0.9mol,而1mol重水中含10mol中子,故0.9mol重水中含有的中子数为9NA个,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
7.下列有关化学用语表示正确的是( )
| A. | 乙烯的结构简式:CH2CH2 | B. | 乙酸的结构式:CH3COOH | ||
| C. | 2-丁烯的键线式: | D. | 乙醇分子的比例模型: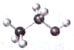 |
8.25℃,向20mL 0.1mol•L-1的H3PO2溶液中滴加0.1mol•L-1的NaOH溶液(滴定过程中溶液温度保持不变),滴定曲线如图1,含磷物种浓度所占分数(δ)随pH变化关系如图2,则下列说法不正确的是( )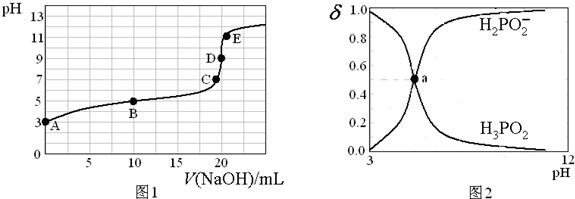

| A. | H3PO2的电离方程式为:H3PO2?H2PO2-+H+;电离常数Ka≈10-5 | |
| B. | B点溶液中存在关系:2c(H+)+c(H3PO2)=2c(OH-)+c(H2PO2-) | |
| C. | 图2中的a点对应为 图1中的B点 | |
| D. | D点时,溶液中微粒浓度大小关系为:c(Na+)>c(H2PO2-)>c(OH-)>c(H+) |
12.对下列有机反应类型的认识,错误的是( )
| A. | CH3CH2OH+CH3COOH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;酯化反应 | |
| B. | CH2=CHCH3+Br2$\stackrel{光照}{→}$CH2=CHCH2Br+HBr;加成反应 | |
| C. | 2CH3CH2OH+O2→2CH3CHO+2H2O;氧化反应 | |
| D. |  +Br2$\stackrel{FeBr_{3}}{→}$ +Br2$\stackrel{FeBr_{3}}{→}$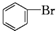 +HBr;取代反应 +HBr;取代反应 |
2.互为同分异构体的物质不可能( )
| A. | 具有相同的相对分子质量 | B. | 具有相同的分子式 | ||
| C. | 具有相同的组成元素 | D. | 具有相同的熔、沸点 |
6.下列各种说法中正确的是( )
| A. | 乙烯和甲苯都能使酸性高锰酸钾溶液褪色 | |
| B. | 凡是能起银镜反应的物质一定是醛 | |
| C. | 在酯化反应中,羧酸脱去羧基中的氢原子,醇脱去羟基生成水和酯 | |
| D. | 苯酚有弱酸性,因此它是一种羧酸 |
 图为实验室某浓硫酸试剂瓶上的标签,试根据有关数据回答下列问题:
图为实验室某浓硫酸试剂瓶上的标签,试根据有关数据回答下列问题: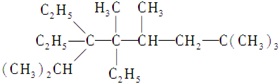 2,2,4,5,7,7-六甲基-3,3,4-乙基辛烷,
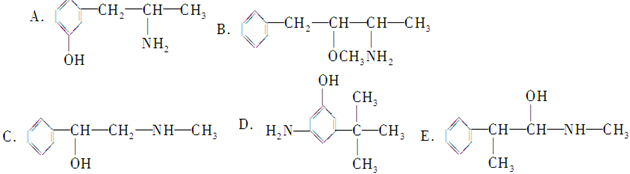
2,2,4,5,7,7-六甲基-3,3,4-乙基辛烷, 下列各物质:与麻黄素互为同分异构体的是DE(填字母)
下列各物质:与麻黄素互为同分异构体的是DE(填字母)