题目内容
20. 在恒容密闭容器中加入一定量的反应物后发生可逆反应:CO(g)+H2O(g)?CO2(g)+H2(g),平衡时 CO2(g)的物质的量浓度c(CO2)与温度T的关系如
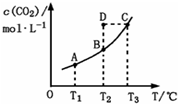
在恒容密闭容器中加入一定量的反应物后发生可逆反应:CO(g)+H2O(g)?CO2(g)+H2(g),平衡时 CO2(g)的物质的量浓度c(CO2)与温度T的关系如图所示.下列说法不正确的是( )
| A. | 反应CO(g)+H2O(g)?CO2(g)+H2(g)的△H>0 | |
| B. | 在T2 时,若反应处于状态D,则一定有v正<v逆 | |
| C. | 平衡状态A 与C 相比,平衡状态A 的c(CO)小 | |
| D. | 若T1、T2时的平衡常数分别为K1、K2,则K1<K2 |
分析 A、由图可知,温度越高平衡时c(CO2)越大,说明升高温度平衡向正反应移动;
B、T2时反应进行到状态D,c(CO2)高于平衡浓度,故反应向逆反应进行;
C、根据温度对平衡的影响,分析平衡状态c(CO);
D、温度越高平衡时c(CO2)越大,说明升高温度平衡向正反应移动.
解答 解:A、由图可知,温度越高平衡时c(CO)越大,说明升高温度平衡向正反应移动,升高温度平衡向吸热反应进行,故正反应是吸热反应,即△H>0,故A正确;
B、T2时反应进行到状态D,c(CO)高于平衡浓度,故反应向逆反应进行,则一定有υ(正)<υ(逆),故B正确;
C、平衡状态A与C相比,C点温度高,已知△H>0,升高温度平衡正移,CO浓度减小,所以A点CO浓度大,故C错误;
D、温度越高平衡时c(CO2)越大,说明升高温度平衡向正反应移动,则温度越高,平衡常数越大,所以T1、T2时的平衡常数分别为K1、K2,则K1<K2,故D正确;
故选C.
点评 本题以化学平衡图象为载体,考查温度对平衡移动的影响、对化学平衡常数的影响等,难度中等,注意曲线的各点都处于平衡状态,注意B选项若有一点不在曲线上,不能单独通过改变温度实现平衡状态的转化.

练习册系列答案
相关题目
10.下列各组物质按酸、碱、盐、电解质分类顺序排列的是( )
| A. | 硫酸、纯碱、明矾、二氧化硫 | B. | 硝酸、烧碱、碳酸钙、氯化钠 | ||
| C. | 醋酸、苛性钠、碳酸钠、氨水 | D. | 盐酸、熟石灰、苛性钠、乙醇 |
8.将下列各组物质按酸、碱、盐分类顺次排列,其中正确的是( )
| A. | 硫酸 纯碱 烧碱 | B. | 硝酸 烧碱 氯化钠 | ||
| C. | 醋酸 酒精 碳酸钙 | D. | 盐酸 熟石灰 苛性钠 |
15.在下列状态下,能导电的电解质是( )
| A. | 硝酸钾溶液 | B. | 液态氯化氢 | C. | 液态水银 | D. | 熔融氯化钠 |
12.氧化铝熔点很高,常用于制造耐火材料,例如制作坩埚,下列操作不能在氧化铝坩埚中进行的是( )
| A. | 加热使CuSO4•5H2O失水 | B. | 加热使KMnO4分解 | ||
| C. | 加热熔化烧碱 | D. | 加热分解碱式碳酸铜 |
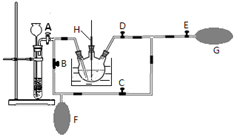 高锰酸钾是一种用途广泛的强氧化剂,实验室制备高锰酸钾所涉及的化学方程式如下:
高锰酸钾是一种用途广泛的强氧化剂,实验室制备高锰酸钾所涉及的化学方程式如下: