题目内容
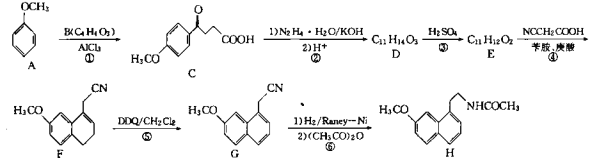
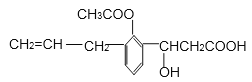
【题目】已知有机物D的相对分子质量为86,将8.6gD完全燃烧的产物依次通过装有浓硫酸和碱石灰的装置,浓硫酸增重9g,碱石灰增重22g。其相关反应如图所示,其中B、D的结构中均含有2个-CH3,它们的核磁共振氢谱中均出现4个峰,且D分子中含有一个醛基。
![]()
请回答:
(1)B中所含官能团的名称为__。
(2)Ⅲ的反应类型为__(填字母序号)。
a.还原反应 b.加成反应 c.氧化反应 d.消去反应
(3)写出下列反应的化学方程式:
Ⅰ:__;Ⅲ:__。
(4)A的同分异构体中有一对互为顺反异构且结构中有2个-CH3,它们的结构简式分别为__和_。
【答案】溴原子 c (CH3)2CHCH2CH2Br+NaOH![]() (CH3)2CHCH=CH2+NaBr+H2O 2(CH3)2CHCH2CH2OH+O2
(CH3)2CHCH=CH2+NaBr+H2O 2(CH3)2CHCH2CH2OH+O2![]() 2(CH3)2CHCH2CHO+2H2O
2(CH3)2CHCH2CHO+2H2O 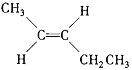
【解析】
有机物D的相对分子质量为86,8.6gD的物质的量![]() ,浓硫酸吸收的是水,碱石灰吸收的是二氧化碳,水的物质的量
,浓硫酸吸收的是水,碱石灰吸收的是二氧化碳,水的物质的量![]() ,二氧化碳的物质的量
,二氧化碳的物质的量![]() ,则有机物D、二氧化碳和水的物质的量之比为
,则有机物D、二氧化碳和水的物质的量之比为![]() ,所以该有机物分子中含有5个碳原子、10个氢原子,D的相对分子质量是86,
,所以该有机物分子中含有5个碳原子、10个氢原子,D的相对分子质量是86,![]() ,所以该分子中还含有1个氧原子,D的分子式为
,所以该分子中还含有1个氧原子,D的分子式为![]() ;D的结构中含有2个
;D的结构中含有2个![]() ,它的核磁共振氢谱中出现4个峰,说明该有机物中含4种类型的氢原子,且含有一个
,它的核磁共振氢谱中出现4个峰,说明该有机物中含4种类型的氢原子,且含有一个![]() ,则D为
,则D为![]() ;C发生氧化反应得到D,则C为
;C发生氧化反应得到D,则C为![]() ,C和
,C和![]() 发生取代反应生成B,B结构中含有2个
发生取代反应生成B,B结构中含有2个![]() ,则B为
,则B为![]() ,B发生消去反应生成A为
,B发生消去反应生成A为![]() 。
。
(1)B为![]() ,B中所含官能团的名称为溴原子;
,B中所含官能团的名称为溴原子;
(2)反应Ⅰ为消去反应、Ⅱ为取代反应、Ⅲ为氧化反应,故选c;
(3)反应Ⅰ的化学方程式为![]() ,反应Ⅲ的化学方程式为
,反应Ⅲ的化学方程式为![]() ;
;
(4)A的同分异构体中有一对互为顺反异构,且结构中有2个![]() ,它们的结构简式分别为
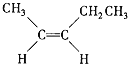
,它们的结构简式分别为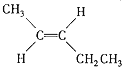 、
、 。
。

 优等生题库系列答案
优等生题库系列答案【题目】据公安部2019年12月统计,2019年全国机动车保有量已达3.5亿。汽车尾气排放的碳氢化合物、氮氧化物及碳氧化物是许多城市大气污染的主要污染物。
I.汽油燃油车上安装三元催化转化器,可有效降低汽车尾气污染。
(1)已知:C(s)+O2(g)=CO2(g) △H1=393.5kJ·mol1
2C(s)+O2(g)=2CO(g) △H2=221.0kJ·mol1
N2(g)+O2(g)=2NO(g) △H3=+180.5kJ·mol1
CO和NO两种尾气在催化剂作用下生成N2的热化学方程式___。
(2)对于2NO(g)+2CO(g)![]() N2(g)+2CO2(g),在一定温度下,于1L的恒容密闭容器中充入0.1molNO和0.3molCO,反应开始进行。
N2(g)+2CO2(g),在一定温度下,于1L的恒容密闭容器中充入0.1molNO和0.3molCO,反应开始进行。
下列能说明该反应已经达到平衡状态的是___(填字母代号)。
A.![]() 比值不变
比值不变
B.容器中混合气体的密度不变
C.v(N2)正=2v(NO)逆
D.容器中混合气体的平均摩尔质量不变
(3)使用间接电化学法可处理燃煤烟气中的NO,装置如图2所示。
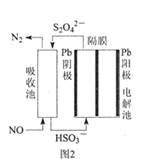
已知电解池的阴极室中溶液的pH在4~7之间,写出阴极的电极反应式__。用离子方程式表示吸收池中除去NO的原理___。
(4)T1温度时在容积为2L的恒容密闭容器中发生反应:2CO(g)+O2(g)![]() 2CO2(g) △H<0。实验测得:v正=v(CO)消耗=2v(O2)消耗=k正c2(CO)·c(O2),v逆=(CO2)消耗=k逆c2(CO2),k正、k逆为速率常数只受温度影响。不同时刻测得容器中n(CO)、n(O2)如表:
2CO2(g) △H<0。实验测得:v正=v(CO)消耗=2v(O2)消耗=k正c2(CO)·c(O2),v逆=(CO2)消耗=k逆c2(CO2),k正、k逆为速率常数只受温度影响。不同时刻测得容器中n(CO)、n(O2)如表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(CO)/mol | 2 | 1.2 | 0.8 | 0.4 | 0.4 | 0.4 |
n(O2)/mol | 1.2 | 0.8 | 0.6 | 0.4 | 0.4 | 0.4 |
①T1温度时![]() =___L/mol。
=___L/mol。
②若将容器的温度改变为T2时其k正=k逆,则T2__T1(填“>”、“<”或“=")。
II.“低碳经济”备受关注,CO2的有效开发利用成为科学家研究的重要课题。在0.1MPa、Ru/TiO2催化下,将一定量的H2和CO2置于恒容密闭容器中发生反应X:CO2(g)+4H2(g) ![]() CH4(g)+2H2O(g) △H<0
CH4(g)+2H2O(g) △H<0
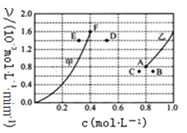
(5)为探究反应X的反应速率与浓度的关系,向恒容密闭容器中通入浓度均为1.0molL-1的H2与CO2。恒温条件下,根据相关数据绘制出反应速率与浓度关系曲线:v正~c(CO2)和v逆~c(H2O)。则与曲线v正~c(CO2)相对应的是如图___曲线。(填“甲”或“乙”);该反应达到平衡后,某一时刻降低温度,反应重新达到平衡,则此时曲线乙对应的平衡点可能为___(填字母)。
(6)温度为T时,向10L密闭容器中充入5molH2和CO2的混合气体,此时容器内压强为5P,两种气体的平衡转化率ɑ与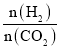 的关系如图所示:
的关系如图所示:
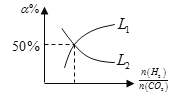
①图中CO2的平衡转化率可用表示___(L1或L2)
②该温度下,反应X的平衡常数Kp=___。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
【题目】ZnSO47H2O可用于测定钢铁及炉渣的含硫量。某工厂下脚料中含锌、镉(Cd)、铜、铁等金属,以该下脚料为原料制备ZnSO47H2O并回收Cu、Cd的工艺流程如图所示:
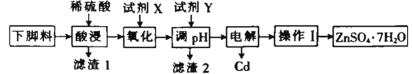
已知部分氢氧化物开始及完全沉淀的pH如表所示(起始时金属离子浓度按0.1molL-1计算):
氢氧化物 | Fe(OH)3 | Cd(OH)2 | Zn(OH)2 |
开始沉淀的 pH | 1.9 | 7.4 | 6.2 |
完全沉淀的 pH | 3.2 | 9.5 | 8.2 |
请回答下列问题:
(1)滤渣1中含有_______(填化学式)。
(2)试剂X是双氧水时,写岀氧化过程中发生反应的离子方程式_______。
(3)pH的调控范围是_______,试剂Y可选用_______(填字母)
A. NaOH B. ZnO C. ZnCO3
(4)电解时以汞(Hg)作电极可以将镉与锌完全分离,镉单质在_______(填“阴”或“阳”)极析出,阳极的电极反应式为_______。
(5)操作I包括的操作是_______及过滤等,过滤后得到的滤液可以加入_______ (填“酸浸”或“氧化”)步骤循环利用。