题目内容
【题目】下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素。请根据要求回答问题:
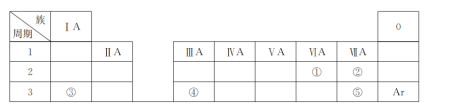
(1)①的元素符号是________;
(2)②和⑤的原子半径大小关系是②________⑤(填“>”“<”或“=”);
(3)③和⑤形成的化合物含有的化学键是__________(填“离子键”或“共价键”);
(4)③、④的最高价氧化物对应的水化物相互反应的离子方程式为_________________________。
【答案】O < 离子键 OH-+Al(OH)3=AlO2-+2H2O
【解析】
根据元素在周期表的位置可知,①②③④⑤对应的元素分别为:O、F、Na、Al和Cl,再结合元素周期律,分析作答。
(1)①的元素符号是O,
故答案为:O;
(2)同主族中,从上到下元素原子的半径依次增大,则②和⑤的原子半径大小关系是②<⑤,
故答案为:<;
(3)③和⑤形成的化合物为氯化钠,由钠离子与氯离子构成,属于离子化合物,含有的化学键为离子键,
故答案为:离子键;
(4)③、④的最高价氧化物对应的水化物分别是氢氧化钠与氢氧化铝,两者会发生反应,其离子方程式为:OH-+Al(OH)3=AlO2-+2H2O,
故答案为:OH-+Al(OH)3=AlO2-+2H2O。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目