��Ŀ����
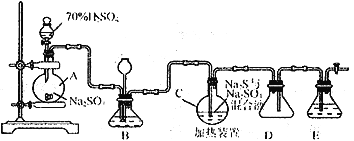
����Ŀ���ϳ�ҽ������ҩ��������E��ʳƷ������J��·����ͼ��ʾ��

��֪��
��ش��������⣺
��1��A���ڷ��������ṹ��ʽΪ_____________��
��2��E�й����ŵ������ǰ�����____________��
��3��C����NaHCO3��Һ��Ӧ����Ӧ�۵Ļ�ѧ����ʽ��___________��
��4����Ӧ�ޡ������Լ�ii���Լ�iii������ ___________��___________��
��5����Ӧ��~���У�����ȡ����Ӧ����_______________��
��6��J�ж���ͬ���칹�壬���з�������������ͬ���칹����______________�֣�д��������һ��ͬ���칹��Ľṹ��ʽ��___________��
a. Ϊ���Ķ�Ԫȡ�������һ��ȡ����Ϊ�ǻ�
b. �������࣬���ܷ���������Ӧ
��7����AΪ��ʼԭ�ϣ�ѡ�ñ�Ҫ�����Լ��ϳɸ߷�����֬�� ����д���ϳ�·�ߣ��ýṹ��ʽ��ʾ�л���ü�ͷ��ʾת����ϵ����ͷ��ע���Լ��ͷ�Ӧ��������_______________��
����д���ϳ�·�ߣ��ýṹ��ʽ��ʾ�л���ü�ͷ��ʾת����ϵ����ͷ��ע���Լ��ͷ�Ӧ��������_______________��
���𰸡� ![]() ����������
���������� ![]() ���Ը��������Һ NaOH/H2O �٢ۢݢ� 6 �����½ṹ��дһ�֣�
���Ը��������Һ NaOH/H2O �٢ۢݢ� 6 �����½ṹ��дһ�֣�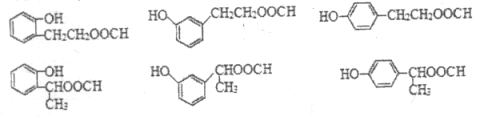
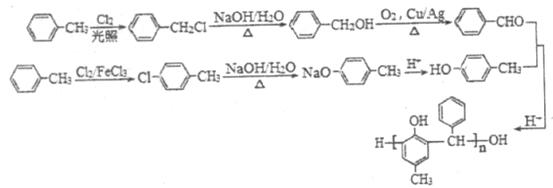
��·�ߺ������ɣ�
��������������������⿼���л��ƶϺ��л��ϳɣ��漰�л�������ŵ�ʶ���л���ṹ��ʽ���л���Ӧ����ʽ����д���л���Ӧ���͵��жϣ���������ͬ���칹����Ŀ��ȷ������д���л��ϳ�·�ߵ���ơ�A���ڷ�������A������Ӧ������B��A�Ľṹ��ʽΪ![]() ���Ա�B��E�Ľṹ��ʽ�Լ���Ӧ������������Ӧ���ǽ�-NO2��ԭΪ-NH2��D�Ľṹ��ʽΪ
���Ա�B��E�Ľṹ��ʽ�Լ���Ӧ������������Ӧ���ǽ�-NO2��ԭΪ-NH2��D�Ľṹ��ʽΪ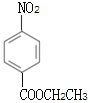 ��C����NaHCO3��Һ��Ӧ��C�к��Ȼ�����Ӧ��Ϊ�����Ը��������Һ��B��-CH3������-COOH��C�Ľṹ��ʽΪ
��C����NaHCO3��Һ��Ӧ��C�к��Ȼ�����Ӧ��Ϊ�����Ը��������Һ��B��-CH3������-COOH��C�Ľṹ��ʽΪ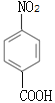 ����Ӧ��ΪC��CH3CH2OH��������Ӧ���Լ�iΪCH3CH2OH��Ũ���������F�ķ���ʽ����Ӧ��ΪA��Cl2�ڴ��������·��������ϵ�ȡ����Ӧ������J�������������ڶ�λ����F�Ľṹ��ʽΪ
����Ӧ��ΪC��CH3CH2OH��������Ӧ���Լ�iΪCH3CH2OH��Ũ���������F�ķ���ʽ����Ӧ��ΪA��Cl2�ڴ��������·��������ϵ�ȡ����Ӧ������J�������������ڶ�λ����F�Ľṹ��ʽΪ![]() �� �����Լ�iΪCH3CH2OH��Ũ���ᣬ��J���Ƴ�I�Ľṹ��ʽΪ
�� �����Լ�iΪCH3CH2OH��Ũ���ᣬ��J���Ƴ�I�Ľṹ��ʽΪ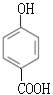 ���Ա�F��I�Ľṹ��ʽ��Fת��ΪI��Ҫ��-CH3������-COOH����-Clˮ��ɷ��ǻ������ڷ��ǻ�Ҳ����������Ӧ��Ϊ�˱������ǻ�������������Ӧ��Ϊ������Ӧ����Ӧ��Ϊˮ�ⷴӦ�����Լ�iiΪ����KMnO4��Һ��G�Ľṹ��ʽΪ
���Ա�F��I�Ľṹ��ʽ��Fת��ΪI��Ҫ��-CH3������-COOH����-Clˮ��ɷ��ǻ������ڷ��ǻ�Ҳ����������Ӧ��Ϊ�˱������ǻ�������������Ӧ��Ϊ������Ӧ����Ӧ��Ϊˮ�ⷴӦ�����Լ�iiΪ����KMnO4��Һ��G�Ľṹ��ʽΪ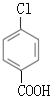 ���Լ�iiiΪNaOH��Һ��H�Ľṹ��ʽΪ
���Լ�iiiΪNaOH��Һ��H�Ľṹ��ʽΪ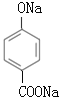 ��
��
��1��A���ڷ�������A�Ľṹ��ʽΪ![]() ��
��
��2����E�Ľṹ��ʽ��֪��E�й����ŵ�����Ϊ������������
��3��C�Ľṹ��ʽΪ ����Ӧ��ΪC��CH3CH2OH��������Ӧ����Ӧ�Ļ�ѧ����ʽΪ��
����Ӧ��ΪC��CH3CH2OH��������Ӧ����Ӧ�Ļ�ѧ����ʽΪ�� +CH3CH2OH
+CH3CH2OH![]()
 +H2O��
+H2O��
��4����Ӧ���ǽ�![]() ��-CH3������-COOH���Լ�ii�����Ը��������Һ����Ӧ����
��-CH3������-COOH���Լ�ii�����Ը��������Һ����Ӧ���� ��ˮ�ⷴӦ���Լ�iii��NaOH��Һ��
��ˮ�ⷴӦ���Լ�iii��NaOH��Һ��
��5����Ӧ��~������Ϊȡ����Ӧ��������Ӧ��ȡ����Ӧ����ԭ��Ӧ��ȡ����Ӧ��������Ӧ��ȡ����Ӧ������ȡ����Ӧ�����٢ۢݢ���
��6��J�Ľṹ��ʽΪ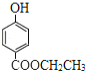 ��J��ͬ���칹�������������ܷ���������Ӧ����ṹ�к���HCOO-��J��ͬ���칹��Ϊ���Ķ�Ԫȡ�������һ��ȡ����Ϊ-OH������������ͬ���칹��������1��������ȡ����Ϊ-OH��-CH2CH2OOCH�����ڡ��䡢������λ�ã��ṹ��ʽΪ
��J��ͬ���칹�������������ܷ���������Ӧ����ṹ�к���HCOO-��J��ͬ���칹��Ϊ���Ķ�Ԫȡ�������һ��ȡ����Ϊ-OH������������ͬ���칹��������1��������ȡ����Ϊ-OH��-CH2CH2OOCH�����ڡ��䡢������λ�ã��ṹ��ʽΪ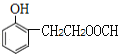 ��
��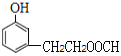 ��
��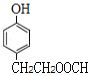 ����2��������ȡ����Ϊ-OH��-CH��CH3��OOCH�����ڡ��䡢������λ�ã��ṹ��ʽΪ
����2��������ȡ����Ϊ-OH��-CH��CH3��OOCH�����ڡ��䡢������λ�ã��ṹ��ʽΪ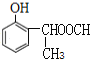 ��
��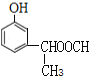 ��
��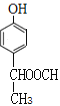 ������������ͬ���칹�干6�֡�
������������ͬ���칹�干6�֡�
��7��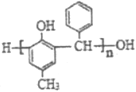 �ɵ���
�ɵ���![]() ��
��![]() �������۷�Ӧ�Ƶã��ϳ�
�������۷�Ӧ�Ƶã��ϳ� ��Ҫ��
��Ҫ��![]() �ϳ�
�ϳ�![]() ��
��![]() ����
����![]() �ϳ�
�ϳ�![]() ����Ҫ��-CH3�Ķ�λ����-OH������
����Ҫ��-CH3�Ķ�λ����-OH������![]() ��Cl2�ڴ��������·��������ϵ�ȡ����Ӧ����
��Cl2�ڴ��������·��������ϵ�ȡ����Ӧ����![]() ��Ȼ��
��Ȼ��![]() ��NaOH��Һ�з���ˮ�ⷴӦ����
��NaOH��Һ�з���ˮ�ⷴӦ����![]() ��
��![]() �ữ��
�ữ��![]() ����
����![]() �ϳ�
�ϳ�![]() ���ڲ�������������ţ�����
���ڲ�������������ţ�����![]() ��Cl2�ڹ����·��������ϵ�ȡ����Ӧ����
��Cl2�ڹ����·��������ϵ�ȡ����Ӧ����![]() ��
��![]() ��NaOH��Һ�з���ˮ�ⷴӦ����
��NaOH��Һ�з���ˮ�ⷴӦ����![]() ��
��![]() ��������������
��������������![]() ���ϳ�·��Ϊ��
���ϳ�·��Ϊ��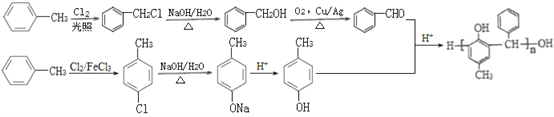 ��
��

 ֥�鿪���γ�������ϵ�д�
֥�鿪���γ�������ϵ�д� ����ѧ��ţ��Ӣ��ϵ�д�
����ѧ��ţ��Ӣ��ϵ�д�