题目内容
【题目】常温下,几种弱电解质的pK(pK=-lgK)如下表所示:

请回答下列问题:
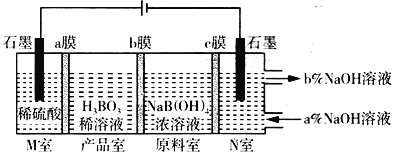
(1)硼酸(H3BO3)在水中存在电离平衡:H3BO3+H2O![]() B(OH)4-+H+。由此推断,硼酸是___(填字母)。
B(OH)4-+H+。由此推断,硼酸是___(填字母)。
A.一元酸 B.三元酸 C.强酸 D.弱酸
(2)常温下,在H3BO3、HN3、H2CrO4中酸性最强的是___(填化学式)。
(3)H2CrO4的二级电离常数表达式Ka2=___。
(4)甲胺在水中的电离和NH3类似,写出CH3NH2在水中的电离方程式:___。
(5)常温下,20mLpH=2的HN3溶液与xmLpH=12的NaOH溶液恰好完全反应,则x___(填“>”“<”或“=”)20mL。
【答案】AD H2CrO4 ![]() CH3NH2+H2O
CH3NH2+H2O![]() CH3NH3++OH- >
CH3NH3++OH- >
【解析】
(1)部分电离的酸是弱酸,只发生一步电离的酸为一元酸,根据电离方程式知,硼酸只发生一步电离且部分电离,所以为一元弱酸,
故选AD;
(2)弱酸的电离平衡常数越大,酸的酸性越强,电离平衡常数:H2CrO4>HN3>H3BO3,所以酸性H2CrO4>HN3>H3BO3,
故答案为:H2CrO4;
(3)H2CrO4的二级电离常数表达式Ka2=![]() ,
,
故答案为:![]() ;
;
(4)甲胺(CH3NH2)类似于氨,但碱性稍强于氨,说明甲胺也是弱电解质,在水溶液中部分电离,其电离方程式为CH3NH2+H2O![]() CH3NH3++OH-,
CH3NH3++OH-,
故答案为:CH3NH2+H2O![]() CH3NH3++OH-;
CH3NH3++OH-;
(5)pH=2的HN3溶液浓度大于0.01mol·L-1,pH=12的NaOH溶液浓度等于0.01mol·L-1,HN3是一元酸、NaOH是一元碱,则常温下20 mL pH=2的HN3溶液与x mL pH=12的NaOH溶液恰好完全反应,说明酸碱的物质的量相等,所以消耗的碱溶液体积大于酸体积,则x>20mL,
故答案为:>。

 全能练考卷系列答案
全能练考卷系列答案