题目内容
甲醇燃料电池可用于笔记本电脑等,它一极通入氧气,另一极通入甲醇;电解质能传导H+。电池工作时, 2CH3OH+3O2 = 2CO2+4H2O ,下列说法正确的是
| A.通甲醇一极为正极。 |
| B.正极电极反应式 3O2 + 12H+ + 12e- = 6H2O |
| C.电池工作时电子从氧气一极流向甲醇一极。 |
| D.当转移24mol e-时,消耗的甲醇2mol。 |
B
关于燃料电池的工作原理:通入燃料的一极为负极,即电子流出的一极,发生氧化反应的一极,阴离子移向的一极;通入空气(或氧化)的一极为正极,即电子流入的一极,发生还原反应的一极;所以
A错,通甲醇的一极为负极;B正确,正极为氧气得电子,在酸性电解质中其电极反应式为:3O2 + 12H+ + 12e- = 6H2O;C错,电子的流向为由负级经导线流向正极;D错,根据氧化还原反应中,得失电子数相等的原则,可得当转移24mol e-时,消耗的甲醇4mol。
A错,通甲醇的一极为负极;B正确,正极为氧气得电子,在酸性电解质中其电极反应式为:3O2 + 12H+ + 12e- = 6H2O;C错,电子的流向为由负级经导线流向正极;D错,根据氧化还原反应中,得失电子数相等的原则,可得当转移24mol e-时,消耗的甲醇4mol。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
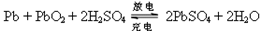 ,下列说法正确的是
,下列说法正确的是 
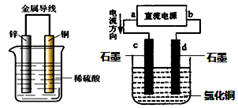

 用的是普通锌-锰电池,请写出该电池工作时发生的
用的是普通锌-锰电池,请写出该电池工作时发生的 (2)汽车上使用的是Pb-PbO2-H2SO4构成的可反复使用的蓄电池,请写出该电池工作时
(2)汽车上使用的是Pb-PbO2-H2SO4构成的可反复使用的蓄电池,请写出该电池工作时