��Ŀ����
9������һ�ַ�����Ԫ�أ������ڶ���ͬλ�أ���${\;}_{92}^{235}$U��${\;}_{92}^{238}$U����������ԭ�ӵ������ʣ�1999�걱Լ��ը������ʱ��ʹ�õ�ƶ�˵��оͺ����ᣬ��������������˺����壬��������Ⱦ�����������б仯${\;}_{92}^{235}$U=${\;}_{82}^{207}$Pb+${\;}_{10}^{20}$Ne+8X����Ԫ�ص�ƽ�����ԭ������Ϊ238.20�����������������ó��Ľ�����ȷ���ǣ�������| A�� | ��Ԫ��һ�����ٻ�����һ������������238��ͬλ�أ�XΪ���� | |
| B�� | �����������������˵�ͬλ�ص����ԭ�������������Ľ������ԭ��������XΪԭ�� | |
| C�� | ǭU�ı仯���ڻ�ѧ�仯��XΪ���� | |
| D�� | �˵ļ���ͬλ�صĻ�ѧ�������Բ�ͬ��XΪ���� |
���� A��Ԫ�ص����ԭ�������������ͬλ�����ԭ�������ļ�Ȩƽ��ֵ��
B��ͬλ�ص����������ڸ�ԭ�ӵĽ������ԭ������
C���÷�Ӧ�Ǻ˷�Ӧ����Ϊ��ѧ�仯ǰ��ԭ�ӵ�����������������ı䣻
D��ͬλ�صĻ�ѧ�������ƣ�
��� �⣺A��Ԫ�ص����ԭ�������������ͬλ�����ԭ�������ļ�Ȩƽ��ֵ����Ԫ�ص�ƽ�����ԭ������Ϊ238.20������Ԫ��һ�����ٴ���һ������������238��ͬλ�أ��ñ仯ǰ�����ӵĺ˵�������䣬��XΪ���ӣ���A��ȷ��
B��ͬλ�ص����������ڸ�ԭ�ӵĽ������ԭ���������ñ仯ǰ�����ӵĺ˵�������䣬��XΪ���ӣ���B����
C���÷�Ӧ�Ǻ˷�Ӧ�������ڻ�ѧ�仯����Ϊ��ѧ�仯ǰ��ԭ�ӵ�����������������ı䣻�ñ仯ǰ�����ӵĺ˵�������䣬��XΪ���ӣ���C����
D��ͬλ�صĻ�ѧ�������ƣ��ñ仯ǰ�����ӵĺ˵�������䣬��XΪ���ӣ���D����
��ѡA��
���� ���⿼��ͬλ�ؼ��˷�Ӧ�����֪ʶ���ѶȲ���Ҫע��Ԫ�ص����ԭ�������������ͬλ�����ԭ�������ļ�Ȩƽ��ֵ����ѧ�仯ǰ��ԭ�ӵ�����������������ı䣮

��ϰ��ϵ�д�
 ���ٴ�����ɽ����ϵ�д�
���ٴ�����ɽ����ϵ�д�
�����Ŀ
20����������ʵ��϶����ܻ�óɹ����ǣ�������
| A�� | ��pH��ֽ����Ũ������Ũ���� | |
| B�� | �õ��۵⻯����Һ���ֶ��������Ͷ�����̼ | |
| C�� | �����Ը��������Һ��ȥ������̼�л��е������������� | |
| D�� | ��������ͭƬ��ŨHNO3��Ӧ��ȡ������������ |
17��Mg��Al��Fe���ֽ����ֱ��ͬŨ�ȡ�ͬ�����ϡ���ᷴӦʱ���ų�������������ȣ�������˵������ȷ���ǣ�������
| A�� | ���ֽ��������ʵ������ | |
| B�� | ���ֽ������ܾ����� | |
| C�� | ���ֽ������������ | |
| D�� | �μӷ�Ӧ�����ֽ�����������Ϊ12��9��28 |
14����֪��Ȼ������ͬλ����16O��17O��18O��ˮ�����ͬλ����H��D����ˮ���ӵ�ԭ�������������Ȼ���ˮ���ӿ����У�������
| A�� | 3�� | B�� | 6�� | C�� | 9 �� | D�� | 12�� |
1������ʽΪC3H6Cl2���л��������һ����ԭ�ӱ���ԭ��ȡ�������ɵ�C3H5Cl3������ͬ���칹�壬ԭ�е�C3H6Cl2Ӧ���ǣ�������
| A�� | 1��3-���ȱ��� | B�� | 1��1-���ȱ��� | C�� | 1��2-���ȱ��� | D�� | 2��2-���ȱ��� |
18����Դ�����������뷢չ�ز���ȱ�����ʣ��Դ�ͳ��Դ�������������������������Դ����Դ�����еıȵ��Ǹı�Ŀǰ�ҹ�Ƶ����������������Ч��ʩ��
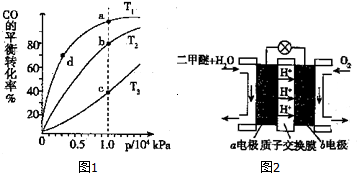
��1���£�N2H4���ͻ��������һ����Ҫ�Ļ���ƽ������������·��Ӿ�����ͬ�ĵ����������߷�Ӧ������������l0e-���ӣ���һ��������Ϊ���ȶ��ĵ��ʣ�д���÷�Ӧ�Ļ�ѧ����ʽN2H4+2H2O2=N2��+4H2O��
��2����ȼú������β�����л��մ����������ڿ��������ĸ��ƣ����ܱ��Ϊ����β�������������漰������Ҫ��Ӧ���£�
��2CO��g��+SO2��g��=S��g��+2CO2��g����H=+8.0kJ•mol-1
��2H2 ��g��+SO2��g��=S��g��+2H2O��g����H=+90.4kJ•mol-1
��2CO��g��+O2��g��=2CO2 ��g����H=-566.0kJ•mol-1l
��2H2 ��g��+O2 ��g��=2H2O��g����H=-483.6kJ•mol-1
S��g����O2��g����Ӧ����SO2 ��g�����Ȼ�ѧ����ʽΪS��g��+O2��g��=SO2 ��g����H=-574kJ•mol-1��
��3��ú̼Һ��Ҳ�����ڼ������������ķ�����Һ����Ӧ֮һΪ��
CO��g��+2H2��g��?CH3OH��g����H��O��������ͬ�����ʵ���Ͷ�ϣ����CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ��ͼ1��ʾ��������Ӧ���ʣ�v��a����v��b����v��c����v��d����С�����˳��Ϊv��d����v��a����v��b����v��c����
ʵ����������������T1�桢1��l04kPa���ң�ѡ���ѹǿ��������ѹǿΪ1��l04kPa���ң�CO��ת�����Ѿ��ܴ�ѹǿ������COת������߲������ɳɱ����ò���ʧ��
��4����ҵ����������Դ�����ѣ�CH3OCH3����ԭ��֮һΪ��
2CO2��g��+6H2�� g��?CH3OCH3��g��+3H2O��g������ͬ�¶��£������������н���������Ӧ��ijʱ���������и���̬���ʵ�Ũ�ȣ�mol•L1-�������淴Ӧ����֮��Ĺ�ϵ���±���ʾ��
��д���пհ״���д�����Ʋ����I����ƽ��״̬����ƽ�ⳣ��k=$\frac{1��1{0}^{-4}����1��1{0}^{-4}��^{3}}{��1��1{0}^{-2}��^{2}����1��1{0}^{-2}��^{6}}$=1������Ũ����Qc=$\frac{1��1{0}^{-4}����2��1{0}^{-4}��^{3}}{��2��1{0}^{-2}��^{2}����1��1{0}^{-2}��^{6}}$=2����Qc��K=1���ʷ�Ӧ���淴Ӧ������У�
��5�������ѣ�ȼ����Ϊ1455kJ/mol��ȼ�ϵ����һ����ɫ��أ��乤��ԭ����ͼ2��ʾ��a��b��Ϊ���Ե缫��a���ĵ缫��ӦʽΪCH3OCH3-12e-+3H2O�T2CO2��+12H+��������1molO2ʱ��ͨ�����ӽ���Ĥ��������Ϊ4NA��
����ع���ʱ����1mol���������ܲ�����������Ϊ1320kJ�����ȼ�ϵ�صĹ���Ч��Ϊ90.7% ��ȼ�ϵ�صĹ���Ч����ָ�������������������ȼ��ȼ��ʱ�����ͷŵ�ȫ������֮�ȣ���

��1���£�N2H4���ͻ��������һ����Ҫ�Ļ���ƽ������������·��Ӿ�����ͬ�ĵ����������߷�Ӧ������������l0e-���ӣ���һ��������Ϊ���ȶ��ĵ��ʣ�д���÷�Ӧ�Ļ�ѧ����ʽN2H4+2H2O2=N2��+4H2O��
��2����ȼú������β�����л��մ����������ڿ��������ĸ��ƣ����ܱ��Ϊ����β�������������漰������Ҫ��Ӧ���£�
��2CO��g��+SO2��g��=S��g��+2CO2��g����H=+8.0kJ•mol-1
��2H2 ��g��+SO2��g��=S��g��+2H2O��g����H=+90.4kJ•mol-1
��2CO��g��+O2��g��=2CO2 ��g����H=-566.0kJ•mol-1l
��2H2 ��g��+O2 ��g��=2H2O��g����H=-483.6kJ•mol-1
S��g����O2��g����Ӧ����SO2 ��g�����Ȼ�ѧ����ʽΪS��g��+O2��g��=SO2 ��g����H=-574kJ•mol-1��
��3��ú̼Һ��Ҳ�����ڼ������������ķ�����Һ����Ӧ֮һΪ��
CO��g��+2H2��g��?CH3OH��g����H��O��������ͬ�����ʵ���Ͷ�ϣ����CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ��ͼ1��ʾ��������Ӧ���ʣ�v��a����v��b����v��c����v��d����С�����˳��Ϊv��d����v��a����v��b����v��c����
ʵ����������������T1�桢1��l04kPa���ң�ѡ���ѹǿ��������ѹǿΪ1��l04kPa���ң�CO��ת�����Ѿ��ܴ�ѹǿ������COת������߲������ɳɱ����ò���ʧ��
��4����ҵ����������Դ�����ѣ�CH3OCH3����ԭ��֮һΪ��
2CO2��g��+6H2�� g��?CH3OCH3��g��+3H2O��g������ͬ�¶��£������������н���������Ӧ��ijʱ���������и���̬���ʵ�Ũ�ȣ�mol•L1-�������淴Ӧ����֮��Ĺ�ϵ���±���ʾ��
| ���� | c��CO2�� | c��H2�� | c��CH3OCH3�� | c��H2O�� | v��������v���棩��С�Ƚ� |
| I | 1.0��10-2 | 1.0��10-2 | 1.0��10-4 | 1.0��10-4 | v������=v���棩 |
| �� | 2.0��10-2 | 1.0��10-2 | 1.0��10-4 | 2.0��10-4 | v�������� v���棩���������=�� |
��5�������ѣ�ȼ����Ϊ1455kJ/mol��ȼ�ϵ����һ����ɫ��أ��乤��ԭ����ͼ2��ʾ��a��b��Ϊ���Ե缫��a���ĵ缫��ӦʽΪCH3OCH3-12e-+3H2O�T2CO2��+12H+��������1molO2ʱ��ͨ�����ӽ���Ĥ��������Ϊ4NA��
����ع���ʱ����1mol���������ܲ�����������Ϊ1320kJ�����ȼ�ϵ�صĹ���Ч��Ϊ90.7% ��ȼ�ϵ�صĹ���Ч����ָ�������������������ȼ��ȼ��ʱ�����ͷŵ�ȫ������֮�ȣ���
19���⡢̼������������Ԫ�ؿ����������Ҫ�Ļ����
��1��һ���¶��£����ܱ������з�Ӧ2NO2��g��?N2O4��g����H��0�ﵽƽ�⣮������������ʱ�����д�ʩ�����NO2ת���ʵ���BC������ĸ����
A����СNO2��Ũ�� B�������¶� C������NO2��Ũ�� D�������¶�
��2���������¡��˹��̵������о��������ڳ��¡���ѹ�����������£�N2�ڴ�������������Fe2O3��TiO2��������ˮ�������з�Ӧ��
N2��g��+3H2O��1��?2NH3��g��+$\frac{3}{2}$O2��g����H=a kJ/mol-1
Ϊ��һ���о�NH3���������¶ȵĹ�ϵ����ó�ѹ�´ﵽƽ��ʱ����ʵ���������±���
�˺ϳɷ�Ӧ��a��0����s��0�������������������=����
��3������Һ���ϳ����صķ�Ӧ�ڽ���ʱ��Ϊ������������һ����2NH3+CO2?H2NCOONH4���ڶ�����H2NCOONH4?H2O+H2NCONH2����һ���Ϊ0.5L�ܱ�������Ͷ��4.0molҺ����1.0mol������̼��ʵ���÷�Ӧ�и������ʱ��ı仯��ͼ1��ʾ��
����֪�ܷ�Ӧ�Ŀ���������һ����������ϳ������ܷ�Ӧ�Ŀ����ɵ�2����Ӧ�������ܷ�Ӧ���е�Լ55 minʱ����ƽ�⣮
�ڷ�Ӧ���е�l0minʱ���CO2�����ʵ�����ͼ��ʾ������CO2��ʾ�ĵ�һ����Ӧ������v��CO2��=0.148 mol/��L•min����
��4����ȼú�����е�CO2ת��Ϊ�����ѵķ�Ӧԭ��Ϊ��2CO2��g��+6H2��g��$\stackrel{����}{?}$CH3OCH3��g��+3H2O��g��
��֪һ�������£��÷�Ӧ��CO2��ƽ��ת�������¶ȡ�Ͷ�ϱ�[n��H2��/n��CO2��]�ı仯������ͼ2��
����������������ʱ��������ͼ�л���ƽ��ʱCH3OCH3�����������Ͷ�ϱ�[n��H2��/n��CO2��]�仯������ͼ��

��5��ֱ���ŷ�úȼ�ղ������������������صĻ������⣮
��úȼ�ղ����������������������CH4����ԭNOx�������������������Ⱦ��
CH4��g��+2NO2��g��=N2��g��+CO2��g��+2H2O��g����H=-867kJ•mol-1
2NO2��g��?N2O4��g����H=-56.9kJ•mol-1
д��CH4����ԭN2O4��g������N2��g����CO2��g����H2O��g�����Ȼ�ѧ����ʽCH4��g��+N2O4��g���TN2��g��+2H2O��g��+CO2��g����H=-810.1kJ/mol��
�ڽ�ȼú�����Ķ�����̼�������ã��ɴﵽ��̼�ŷŵ�Ŀ�ģ���ͼ��ͨ�����ת��ԭ��������ԭ���Ʊ��²�Ʒ��ʾ��ͼ��д���������ת�����̵Ļ�ѧ��Ӧ����ʽ2CO2+2H2O$\frac{\underline{\;����\;}}{\;}$2HCOOH+O2������a��b֮�����ӵ����ϵ�������������a��b����a��b��b��a����
��1��һ���¶��£����ܱ������з�Ӧ2NO2��g��?N2O4��g����H��0�ﵽƽ�⣮������������ʱ�����д�ʩ�����NO2ת���ʵ���BC������ĸ����
A����СNO2��Ũ�� B�������¶� C������NO2��Ũ�� D�������¶�
��2���������¡��˹��̵������о��������ڳ��¡���ѹ�����������£�N2�ڴ�������������Fe2O3��TiO2��������ˮ�������з�Ӧ��
N2��g��+3H2O��1��?2NH3��g��+$\frac{3}{2}$O2��g����H=a kJ/mol-1
Ϊ��һ���о�NH3���������¶ȵĹ�ϵ����ó�ѹ�´ﵽƽ��ʱ����ʵ���������±���
| T/K | 303 | 313 | 323 |
| NH3������/��10-6mol�� | 4.8 | 5.9 | 6.0 |
��3������Һ���ϳ����صķ�Ӧ�ڽ���ʱ��Ϊ������������һ����2NH3+CO2?H2NCOONH4���ڶ�����H2NCOONH4?H2O+H2NCONH2����һ���Ϊ0.5L�ܱ�������Ͷ��4.0molҺ����1.0mol������̼��ʵ���÷�Ӧ�и������ʱ��ı仯��ͼ1��ʾ��

����֪�ܷ�Ӧ�Ŀ���������һ����������ϳ������ܷ�Ӧ�Ŀ����ɵ�2����Ӧ�������ܷ�Ӧ���е�Լ55 minʱ����ƽ�⣮
�ڷ�Ӧ���е�l0minʱ���CO2�����ʵ�����ͼ��ʾ������CO2��ʾ�ĵ�һ����Ӧ������v��CO2��=0.148 mol/��L•min����
��4����ȼú�����е�CO2ת��Ϊ�����ѵķ�Ӧԭ��Ϊ��2CO2��g��+6H2��g��$\stackrel{����}{?}$CH3OCH3��g��+3H2O��g��
��֪һ�������£��÷�Ӧ��CO2��ƽ��ת�������¶ȡ�Ͷ�ϱ�[n��H2��/n��CO2��]�ı仯������ͼ2��
����������������ʱ��������ͼ�л���ƽ��ʱCH3OCH3�����������Ͷ�ϱ�[n��H2��/n��CO2��]�仯������ͼ��

��5��ֱ���ŷ�úȼ�ղ������������������صĻ������⣮
��úȼ�ղ����������������������CH4����ԭNOx�������������������Ⱦ��
CH4��g��+2NO2��g��=N2��g��+CO2��g��+2H2O��g����H=-867kJ•mol-1
2NO2��g��?N2O4��g����H=-56.9kJ•mol-1
д��CH4����ԭN2O4��g������N2��g����CO2��g����H2O��g�����Ȼ�ѧ����ʽCH4��g��+N2O4��g���TN2��g��+2H2O��g��+CO2��g����H=-810.1kJ/mol��
�ڽ�ȼú�����Ķ�����̼�������ã��ɴﵽ��̼�ŷŵ�Ŀ�ģ���ͼ��ͨ�����ת��ԭ��������ԭ���Ʊ��²�Ʒ��ʾ��ͼ��д���������ת�����̵Ļ�ѧ��Ӧ����ʽ2CO2+2H2O$\frac{\underline{\;����\;}}{\;}$2HCOOH+O2������a��b֮�����ӵ����ϵ�������������a��b����a��b��b��a����
 ����Ӧ��NaH��Ϊ��ԭ����
����Ӧ��NaH��Ϊ��ԭ����
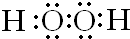 ��CԪ�������ڱ��е�λ���ǵڶ����ڡ��ڢ�A�壮
��CԪ�������ڱ��е�λ���ǵڶ����ڡ��ڢ�A�壮