题目内容
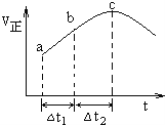
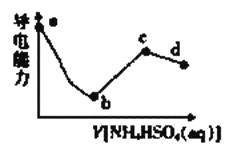
【题目】向一定浓度的Ba(OH)2溶液中滴入某浓度的NH4HSO4溶液,其导电能力随滴入溶液体积的变化如图所示。下列说法正确的是
A.b点溶液中只存在H2O的电离平衡和BaSO4的沉淀溶解平衡
B.c点滚液中:c(H+)+c(NH4+)=c(NH3H2O)+c(OH-)
C.ab段反应的离子方程式为![]()
D.bc段之间存在某点,其溶液中:c(NH4+)=2c(SO42-)
【答案】D
【解析】
A.b点时导电能力最弱,则n(NH4HSO4)=n[Ba(OH)2],溶液中生的反应NH4HSO4+ Ba(OH)2= BaSO4↓+ NH3H2O+H2O,该点中的溶质为NH3H2O,所以b溶液中存在NH3H2O、H2O的电离平衡和BaSO4的沉淀溶解平衡,A项错误;
B.c点时导电能力最强,n(NH4HSO4)=2n[Ba(OH)2],该点溶液中发生的反应为2NH4HSO4+ Ba(OH)2= BaSO4↓+ (NH4)2SO4+2H2O,该点溶液中溶质为(NH4)2SO4,所以根据电荷守恒有:c(H+)+c(NH4+)=2c(SO42-)+c(OH-),溶液2c(SO42-)>c(NH3H2O),因此c(H+)+c(NH4+)> c(NH3H2O)+c(OH-),B项错误;
C.根据以上分析,ab段反生的离子方程式为:NH4++H++SO42-+ Ba2++2OH-= BaSO4↓+ NH3H2O+H2O,C项错误;
D.根据以上分析,b点溶液中的溶质为NH3H2O显碱性,而c点溶液中溶质为(NH4)2SO4,水解显酸性,所以bc段之间存在某点,可以显中性,根据电荷守恒:c(H+)+c(NH4+)=2c(SO42-)+c(OH-),因此c(NH4+)=2c(SO42-),D项正确;
答案选D。

【题目】在相同温度和压强下,对反应CO2(g)+H2(g)![]() CO(g)+H2O(g)进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下表
CO(g)+H2O(g)进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下表
| CO2 | H2 | CO | H2O |
甲 | amol | amol | 0mol | 0mol |
乙 | 2amol | amol | 0mol | 0mol |
丙 | 0mol | 0mol | amol | amol |
丁 | amol | 0mol | amol | amol |
上述四种情况达到平衡后,n(CO)的大小顺序是
A. 乙=丁>丙=甲B. 乙>丁>甲>丙
C. 丁>乙>丙=甲D. 丁>丙>乙>甲
【题目】最近科学家提出“绿色自由”构想:把含有大量CO2的空气吹入碳酸钾溶液中,再把CO2从溶液中提取出来,并使之与氢气反应生成可再生能源甲醇。其工艺流程如图所示:
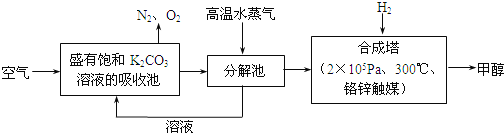
(1)写出分解池中反应的化学方程式为_______________;
(2)在合成塔中,若有4.4kg CO2与足量H2恰好完全反应,生成气态的水和甲醇,可放出4947kJ的热量,试写出该反应的热化学方程式_______________;
(3)已知合成塔中的反应是可逆的,根据平衡移动原理,低温有利于原料气的转化,而实际生产中采用300℃的温度,其原因可能是_______________;
(4)“绿色自由”构想流程中常包括物质的“循环利用”,上述流程中能体现“循环利用”的物质除碳酸钾溶液外,还包括________(化学式)。
(5)300℃时,将CO和H2按1:3的体积比充入密闭容器中,CO2的平衡转化率(α)与体系总压强(p)的关系如图所示。根据图示回答下列问题:
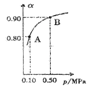
①若其他条件不变,将A点的体积压缩至原来的一半,一段时间后反应再达平衡是,与原平衡比较下列说法正确的是________。
A.CO2的浓度减小 |
B.正反应速率增大,逆反应速率减小 |
C.CO2和H2的体积比为1:3 |
D.CH3OH的体积分数增大 |
②将1.0molCO2和3.0molH2置于体积不变的密闭容器中,2min时反应达到平衡,此时体系总压强为0.10MPa,用H2表示的反应速率为1.2mol/(L·min),则密闭容器的体积是____L。
(6)甲醇可制作燃料电池。以氢氧化钾溶液为电解质的负极反应式是__________。当转移的电子的物质的量为_______mol时,参加反应的氧气的体积是6.72L(标准状况下)。