��Ŀ����
��2010?������һģ��[��ѧ-�л���ѧ����]
A��B��C��D���ַ����廯�����е���ҩ��е������ϣ����ǵĽṹ��ʽ������ʾ��
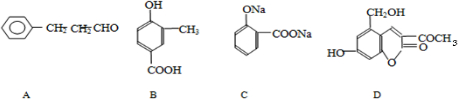
��ش��������⣺
��1������ʹFeCl3��Һ����ɫ���ܺ�NaHCO3��Ӧ�ų��������
��2��1molA�������
��3��B��ͬ���칹���У���������������λȡ�������ֱ�Ϊ��-OH���ͺ��С�-COO-���ṹ�Ļ��Ź���4�֣��������֣�G��H���ṹ��ʽ��ͼ��ʾ���벹���������֣�
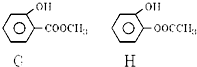

 ��
��
 ��
��
��4��2006����������ڶ���ҩ�������ļ�ҩ����������ע��Һ�����¶�������������˥�ߣ�D�ǡ��������ء��Ľṹ��ʽ�������Ը��ϱ������ܳ���������ٴ�����ҩ��ʹ�����۵Ķ��ʴ���Ϊ���ϣ����ʴ�Ϊ��ҵ�ܼ����к�ǿ�Ķ��ԣ�
��д�����������ء��ķ���ʽ
�ں˴Ź��������������ֶ��ʴ���������3�����շ壬�����֮��Ϊ2��2��1��ͨ�������ⶨ�������ԭ������Ϊ106����֪���ʴ���̼����Ԫ�ص�����������ͬ���������������Ϊ9.43%��1mol���ʴ��������Ľ����Ʒ�Ӧ����1molH2��д�����ʴ��Ľṹ��ʽ
��5���������ڴ��������¿�ֱ�ӷ�Ӧ�����������Ӳ��ܣ���ֻ�ܸ��л�����������������
���磺
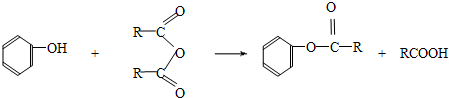
����CΪ����ԭ�ϣ���ѡ���Ҫ��������Ӧ������;���ϳ�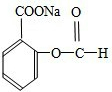
��д���䷴Ӧ�Ļ�ѧ����ʽ��
��
 ����
����
 ��
��
A��B��C��D���ַ����廯�����е���ҩ��е������ϣ����ǵĽṹ��ʽ������ʾ��

��ش��������⣺
��1������ʹFeCl3��Һ����ɫ���ܺ�NaHCO3��Ӧ�ų��������
B
B
����A��B��C��D��գ�����2��1molA�������
4
4
molH2�����ӳɷ�Ӧ����3��B��ͬ���칹���У���������������λȡ�������ֱ�Ϊ��-OH���ͺ��С�-COO-���ṹ�Ļ��Ź���4�֣��������֣�G��H���ṹ��ʽ��ͼ��ʾ���벹���������֣�
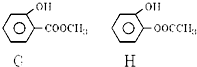




��4��2006����������ڶ���ҩ�������ļ�ҩ����������ע��Һ�����¶�������������˥�ߣ�D�ǡ��������ء��Ľṹ��ʽ�������Ը��ϱ������ܳ���������ٴ�����ҩ��ʹ�����۵Ķ��ʴ���Ϊ���ϣ����ʴ�Ϊ��ҵ�ܼ����к�ǿ�Ķ��ԣ�
��д�����������ء��ķ���ʽ
C12H10O5
C12H10O5
�ں˴Ź��������������ֶ��ʴ���������3�����շ壬�����֮��Ϊ2��2��1��ͨ�������ⶨ�������ԭ������Ϊ106����֪���ʴ���̼����Ԫ�ص�����������ͬ���������������Ϊ9.43%��1mol���ʴ��������Ľ����Ʒ�Ӧ����1molH2��д�����ʴ��Ľṹ��ʽ
HOCH2CH2OCH2CH2OH
HOCH2CH2OCH2CH2OH
����5���������ڴ��������¿�ֱ�ӷ�Ӧ�����������Ӳ��ܣ���ֻ�ܸ��л�����������������
���磺

����CΪ����ԭ�ϣ���ѡ���Ҫ��������Ӧ������;���ϳ�

��д���䷴Ӧ�Ļ�ѧ����ʽ��
��




��������1������ʹFeCl3��Һ����ɫ���ܺ�NaHCO3��Ӧ�ų�������л���Ӧ���з��ǻ����Ȼ���
��2��A�к��б�����ȩ�������������������ӳɷ�Ӧ��
��3������-COO-�����ŵ�ͬ���칹�����Ϊ-CH2COOH��-OOCCH3��-COOCH3��-CH2OOCH�ȣ�
��4���ٸ����������صĽṹ��ʽ�жϺ��е�Ԫ�������ԭ�Ӹ�����������ȷ������ʽ��
�ں˴Ź��������������ֶ��ʴ���������3�����շ壬�����֮��Ϊ2��2��1��ͨ�������ⶨ�������ԭ������Ϊ106����֪���ʴ���̼����Ԫ�ص�����������ͬ���������������Ϊ9.43%����̼����Ԫ�ص����������ֱ�Ϊ
=45.3%��1mol���ʴ��������Ľ����Ʒ�Ӧ����1molH2��˵�������к���2��-OH��
��5��������Һ��ͨ�������̼�������ɷ��ǻ���Ȼ����л�����������������
��2��A�к��б�����ȩ�������������������ӳɷ�Ӧ��
��3������-COO-�����ŵ�ͬ���칹�����Ϊ-CH2COOH��-OOCCH3��-COOCH3��-CH2OOCH�ȣ�
��4���ٸ����������صĽṹ��ʽ�жϺ��е�Ԫ�������ԭ�Ӹ�����������ȷ������ʽ��
�ں˴Ź��������������ֶ��ʴ���������3�����շ壬�����֮��Ϊ2��2��1��ͨ�������ⶨ�������ԭ������Ϊ106����֪���ʴ���̼����Ԫ�ص�����������ͬ���������������Ϊ9.43%����̼����Ԫ�ص����������ֱ�Ϊ
| 1-9.43% |
| 2 |
��5��������Һ��ͨ�������̼�������ɷ��ǻ���Ȼ����л�����������������
����⣺��1������ʹFeCl3��Һ����ɫ���ܺ�NaHCO3��Ӧ�ų�������л���Ӧ���з��ǻ����Ȼ���B���ϣ��ʴ�Ϊ��B��
��2��A�к��б�����ȩ�������������������ӳɷ�Ӧ����1molA�������4molH2�����ӳɷ�Ӧ���ʴ�Ϊ��4��
��3������-COO-�����ŵ�ͬ���칹�����Ϊ-CH2COOH��-OOCCH3��-COOCH3��-CH2OOCH�ȣ��������⣬������ͬ���칹��Ϊ ��
�� ��
��
�ʴ�Ϊ�� ��
�� ��
��
��4�������������к���12��C��10��H��5��O�������ʽΪC12H10O5���ʴ�Ϊ��C12H10O5��
�ں˴Ź��������������ֶ��ʴ���������3�����շ壬�����֮��Ϊ2��2��1��ͨ�������ⶨ�������ԭ������Ϊ106����֪���ʴ���̼����Ԫ�ص�����������ͬ���������������Ϊ9.43%����̼����Ԫ�ص����������ֱ�Ϊ
=45.3%����N��C��=
=4��N��O��=
=3��N��H��=
=10������ʽΪC4H10O3��1mol���ʴ��������Ľ����Ʒ�Ӧ����1molH2��˵�������к���2��-OH����ṹ��ʽӦΪHOCH2CH2OCH2CH2OH��
�ʴ�Ϊ��HOCH2CH2OCH2CH2OH��
��5��������Һ��ͨ�������̼�������ɷ��ǻ���Ȼ����л�������������������Ӧ����ط���ʽΪ ��
�� ��
��
�ʴ�Ϊ���� ����
���� ��
��
��2��A�к��б�����ȩ�������������������ӳɷ�Ӧ����1molA�������4molH2�����ӳɷ�Ӧ���ʴ�Ϊ��4��
��3������-COO-�����ŵ�ͬ���칹�����Ϊ-CH2COOH��-OOCCH3��-COOCH3��-CH2OOCH�ȣ��������⣬������ͬ���칹��Ϊ
 ��
�� ��
���ʴ�Ϊ��
 ��
�� ��
����4�������������к���12��C��10��H��5��O�������ʽΪC12H10O5���ʴ�Ϊ��C12H10O5��
�ں˴Ź��������������ֶ��ʴ���������3�����շ壬�����֮��Ϊ2��2��1��ͨ�������ⶨ�������ԭ������Ϊ106����֪���ʴ���̼����Ԫ�ص�����������ͬ���������������Ϊ9.43%����̼����Ԫ�ص����������ֱ�Ϊ
| 1-9.43% |
| 2 |
| 106��45.3% |
| 12 |
| 106��45.3% |
| 16 |
| 106��9.43% |
| 1 |
�ʴ�Ϊ��HOCH2CH2OCH2CH2OH��
��5��������Һ��ͨ�������̼�������ɷ��ǻ���Ȼ����л�������������������Ӧ����ط���ʽΪ
 ��
�� ��
���ʴ�Ϊ����
 ����
���� ��
�������������ۺϿ����л���ĺϳɣ��������л���ṹ�����ʵĿ��飬���չ����ŵ�����Ϊ������Ĺؼ����״���Ϊͬ���칹����жϣ�ע������ж�˼·��

��ϰ��ϵ�д�
�����Ŀ
 ��2010?������һģ��������ͼ��ʾ��һЩ���ʻ�����Ĵ�����ϵ�����и����в���ȷ���ǣ���������
��2010?������һģ��������ͼ��ʾ��һЩ���ʻ�����Ĵ�����ϵ�����и����в���ȷ���ǣ���������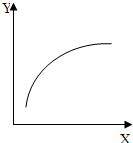 ��2010?������һģ����һ�ܱ�����ͨ��N2��H2����һ�������·�����Ӧ��N2+3H2�T2NH3����0���ﵽƽ���ֻ�ı�����һ��������X������ ����Y���ı仯һ������ͼ�����ߵ��ǣ���������
��2010?������һģ����һ�ܱ�����ͨ��N2��H2����һ�������·�����Ӧ��N2+3H2�T2NH3����0���ﵽƽ���ֻ�ı�����һ��������X������ ����Y���ı仯һ������ͼ�����ߵ��ǣ���������