题目内容
NA为阿伏加德罗常数的数值,下列说法中正确的是( )
| A.恒容加入l.5mol H2和0.5mol N2,充分反应后可得到NH3分子数为NA |
| B.一定条件下,2.3g的Na完全与O2反应生成3.6g产物时失去的电子数为0.1NA |
| C.常温常压下,22.4L Cl2与足量的铁粉反应,转移的电子数为2NA |
| D.标准状况下,22.4L的CH3CHO中含有的分子数为NA |
B
试题分析:合成氨的反应是可逆反应,A不正确,氨气的物质的量小于1mol;钠在反应中不论是生成氧化钠,还是生成过氧化钠,都是失去1个电子的,B正确;常温常压下,22.4L氯气的物质的量不是1mol,C不正确;标准状况下,乙醛不是气态,不能适用于气体摩尔体积,D不正确,答案选B。
点评:阿伏加德罗常数是历年高考的“热点”问题,为高考必考题目,这是由于它既考查了学生对物质的量、粒子数、质量、体积等与阿伏加德罗常数关系的理解,又可以涵盖多角度的化学知识内容。要准确解答好这类题目,一是要掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系;二是要准确弄清分子、原子、原子核内质子中子及核外电子的构成关系。

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
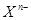 含中子N个,X的质量数为A,则ag X的氢化物中含质子的物质的量是
含中子N个,X的质量数为A,则ag X的氢化物中含质子的物质的量是 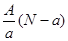 mol
mol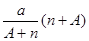 mol
mol mol
mol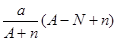 mol
mol
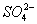 )?之比为 ( )
)?之比为 ( )