题目内容
(2010?江西模拟)下列说法正确的是 ①NaCl晶体中每个Na+同时吸引着8个Cl-,CsCl晶体中每个Cl-同时吸引着6个Cs+②蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质 ③水分子之间存在氢键,所以水受热不易分解 ④胶体的本质特征是丁达尔现象 ⑤除去铁粉中混有的少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤 ⑥可用Ba(OH)2溶液同时鉴别Fe(NO3)3、AlCl3、NH4Cl、FeCl2、Na2SO4五种溶液( )
分析:①根据NaCl晶体、CsCl晶体中氯离子的配位数判断.
②根据强电解质、弱电解质和非电解质的概念判断.
③氢键影响物质的物理性质不影响化学性质.
④丁达尔现象不是胶体的本质特征.
⑤除杂的方法是除去杂质不引进新的杂质,且操作方便可行.
⑥根据能否产生不同现象来区分开.
②根据强电解质、弱电解质和非电解质的概念判断.
③氢键影响物质的物理性质不影响化学性质.
④丁达尔现象不是胶体的本质特征.
⑤除杂的方法是除去杂质不引进新的杂质,且操作方便可行.
⑥根据能否产生不同现象来区分开.
解答:解:①NaCl晶体中每个Na+同时吸引着6个Cl-,CsCl晶体中每个Cl-同时吸引着8个Cs+,故错误.
②硫酸钡虽然难溶于水,但在熔融状态能完全电离,所以属于强电解质;蔗糖在水溶液里以分子存在,属于非电解质;水能部分电离,属于弱电解质,所以蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质,故正确.
③水分子之间存在氢键,导致水的熔沸点较大,水中氧元素的非金属性较强,所以其氢化物较稳定,即水受热不易分解,故错误.
④胶体的本质特征是微粒直径在1-100nm之间,故错误.
⑤铝粉能和氢氧化钠反应生成可溶性的偏铝酸钠,但铁和氢氧化钠不反应,所以除去铁粉中混有的少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤,故正确.
⑥氢氧化钡和硝酸铁反应生成红褐色的氢氧化铁沉淀;和氯化铝反应先生成白色沉淀,当氢氧化钡过量时白色沉淀又溶解;和氯化铵反应生成刺激性气味的气体;和氯化亚铁反应先生成白色絮状沉淀,立即白色沉淀又转变为红褐色沉淀;和硫酸钠反应生成白色沉淀,且氢氧化钡过量时,白色沉淀不消失;所以可用Ba(OH)2溶液同时鉴别Fe(NO3)3、AlCl3、NH4Cl、FeCl2、Na2SO4五种溶液,故正确.
故选A.
②硫酸钡虽然难溶于水,但在熔融状态能完全电离,所以属于强电解质;蔗糖在水溶液里以分子存在,属于非电解质;水能部分电离,属于弱电解质,所以蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质,故正确.
③水分子之间存在氢键,导致水的熔沸点较大,水中氧元素的非金属性较强,所以其氢化物较稳定,即水受热不易分解,故错误.
④胶体的本质特征是微粒直径在1-100nm之间,故错误.
⑤铝粉能和氢氧化钠反应生成可溶性的偏铝酸钠,但铁和氢氧化钠不反应,所以除去铁粉中混有的少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤,故正确.
⑥氢氧化钡和硝酸铁反应生成红褐色的氢氧化铁沉淀;和氯化铝反应先生成白色沉淀,当氢氧化钡过量时白色沉淀又溶解;和氯化铵反应生成刺激性气味的气体;和氯化亚铁反应先生成白色絮状沉淀,立即白色沉淀又转变为红褐色沉淀;和硫酸钠反应生成白色沉淀,且氢氧化钡过量时,白色沉淀不消失;所以可用Ba(OH)2溶液同时鉴别Fe(NO3)3、AlCl3、NH4Cl、FeCl2、Na2SO4五种溶液,故正确.
故选A.
点评:本题考查了的知识点较多,难度不大,易错选项是④,注意胶体的本质特征不是丁达尔现象而是微粒直径的大小.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
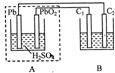 (2010?江西模拟)该图装置中,A为铅蓄电池,C1、C2为石墨电极,B烧杯中是浓度均为0.1mol/L的H2SO3和KI的混合溶液100mL.下列说法正确的是( )
(2010?江西模拟)该图装置中,A为铅蓄电池,C1、C2为石墨电极,B烧杯中是浓度均为0.1mol/L的H2SO3和KI的混合溶液100mL.下列说法正确的是( )