题目内容
9.下列实验操作中正确的是( )| A. | 分液操作时,先将分液漏斗中下层液体从下口放出,再将上层液体从下口放出 | |
| B. | 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 | |
| C. | 蒸馏操作时,应向蒸馏烧瓶中加入几块沸石,以防止暴沸 | |
| D. | 萃取操作时,可以选用CCl4或酒精作为萃取剂从溴水中萃取溴 |
分析 A.分液时应避免液体重新混合而污染;
B.蒸发时,应避免温度过高而导致固体迸溅;
C.加入沸石,可防止液体暴沸;
D.酒精易溶于水,不能用于萃取剂.
解答 解:A.分液时为避免液体重新混合而污染,应先将分液漏斗中下层液体从下口放出,再将上层液体从上口倒出,故A错误;
B.蒸发时,应避免温度过高而导致固体迸溅,应使有大量晶体析出时停止加热,用余热蒸干,故B错误;
C.加入沸石,可防止液体暴沸,故C正确;
D.酒精易溶于水,不能用于萃取剂,可用苯或四氯化碳,故D错误.
故选C.
点评 本题考查混合物分离提纯的方法及选择,为高频考点,把握物质的性质及性质差异为解答的关键,侧重混合物分离方法的考查,题目难度不大.

练习册系列答案
相关题目
19.关于胶体的叙述错误的是( )
| A. | 溶液显电中性,胶体带有电荷,所以胶体较稳定 | |
| B. | 胶体粒子能透过滤纸,但不能透过半透膜,所以可用渗析的方法精制胶体 | |
| C. | 可用丁达尔效应区分溶液和胶体 | |
| D. | 电泳实验说明了胶体粒子能吸附溶液中的阳离子或阴离子而带有电荷 |
20.下列有关钠及其化合物的说法中正确的是( )
| A. | 在Na2SO4、Na2O以及Na2O2中,阳离子与阴离子的个数比均为2:1 | |
| B. | 实验桌上金属钠着火不能用常规灭火器灭火,可以选择用湿布盖灭 | |
| C. | 长距离运输鱼苗,最好在水中加入一定量的Na2O2,以起到供氧和杀菌的作用 | |
| D. | 金属钠和钾都保存在煤油中,所以金属锂(密度为0.534 g/cm3)也应该保存在煤油中 |
17.利用合成气(主要成分为 CO、CO2和 H2)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2(g)?CH3OH(g)△H1=-99kJ?mol-1
②CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H2
③CO2(g)+H2(g)?CO(g)+H2O(g)△H3=+41kJ?mol-1
已知反应①中的相关的化学键键能数据如下,则 C-H 键能和△H2分别是( )
①CO(g)+2H2(g)?CH3OH(g)△H1=-99kJ?mol-1
②CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H2
③CO2(g)+H2(g)?CO(g)+H2O(g)△H3=+41kJ?mol-1
已知反应①中的相关的化学键键能数据如下,则 C-H 键能和△H2分别是( )
| 化学键 | H-H | C-O | C═O | H-O | C-H |
| E/(kJ.mol-1) | 436 | 343 | 1076 | 465 | 413 |
| A. | 403 kJ•mol-1,-66 kJ•mol-1 | B. | 423 kJ•mol-1,+28 kJ•mol-1 | ||
| C. | 314 kJ•mol-1,-18 kJ•mol-1 | D. | 413 kJ•mol-1,-58 kJ•mol-1 |
4.下列组合①氯化铝和氢氧化钠 ②四羟基合铝酸钠和盐酸 ③盐酸和碳酸钠 ④硝酸银和氨水中,因加入的顺序不同,现象不同是( )
| A. | ①② | B. | ①②③ | C. | ①②④ | D. | 全部 |
14.下列对实验操作分析错误的是( )
| A. | 配制0.1mol/L NaCl溶液时,若没有洗涤烧杯和玻璃棒,则所得溶液物质的量浓度偏低 | |
| B. | NH4NO3溶解吸热,若配制0.5mol/L H4NO3溶液时直接将溶解后的溶液转移到容量瓶中,则所得溶液的物质的量浓度偏高 | |
| C. | 配制一定物质的量浓度溶液时,若所用砝码已经生锈,则所得溶液的物质的量浓度偏高 | |
| D. | 配制一定物质的量浓度溶液时,若定容中不小心加水超过刻度线,立刻将超出的水吸出,则所得溶液的物质的量浓度偏低 |
1.下列说法中正确的是( )
| A. | 摩尔既是物质的量的单位又是物质的质量单位 | |
| B. | 物质的量既表示物质的数量又表示物质的质量 | |
| C. | 阿伏加德罗常数是12kg碳12中含有的碳原子数目 | |
| D. | 1molH2O中含有10mol电子 |
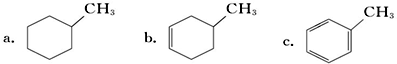 ,属于芳香烃的是c(填字母),它与苯的关系是同系物,写出苯与溴发生反应的化学方程式
,属于芳香烃的是c(填字母),它与苯的关系是同系物,写出苯与溴发生反应的化学方程式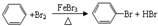 ,预测该芳香烃能(填“能”或“不能”)发生该类反应.
,预测该芳香烃能(填“能”或“不能”)发生该类反应. ,属于取代反应.③由苯制取环己烷:
,属于取代反应.③由苯制取环己烷: ,属于加成反应.
,属于加成反应.