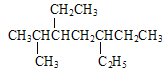题目内容
【题目】冬季下雪后,城市道路常使用融雪剂,其主要成分的 化学式为 XY2,X、Y 均为周期表前 20 号元素,其阳离子和阴离子电子层结构相同,且 1 mol XY2 含有 54 mol 电子。
(1)该融雪剂的化学式是___________,该物质中化学键类型是___________。
(2)元素 D、E 原子的最外层电子数是其电子层数的 2 倍,D 与 Y 相邻,则 D 的 离子结构示意图是___________;D 与 E 能形成一种结构类似于 CO2 的三原子 分子,且每个原子均达到了 8e-稳定结构,该分子的电子式为___________, 化学键类型为___________ (填“离子键”或“共价键”)。
(3)W 是与 D 同主族的短周期元素,Z 是第三周期金属性最强的元素,Z 的单质 在 W 的常见单质中反应时有两种产物:不加热时生成___________,其化学键类型为___________;加热时生成___________,其化学键类型为___________,电子式为___________。
【答案】CaCl2 离子键 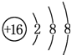
![]() 共价键 Na2O 离子键 Na2O2 离子键和非极性共价键
共价键 Na2O 离子键 Na2O2 离子键和非极性共价键 ![]()
【解析】
X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,含有相同的核外电子数,且1molXY2含有54mol电子,则阴、阳离子核外电子数为![]() =18,为Ca2+、Cl-;元素D、E原子的最外层电子数是其电子层数的2倍,D与氯元素相邻,则D为硫元素;E有2个电子层,最外层电子数为4,则E为碳元素;W是与S同主族的短周期元素,则W为O元素,Z是第三周期金属性最强的元素,则Z为Na,据此分析解答。
=18,为Ca2+、Cl-;元素D、E原子的最外层电子数是其电子层数的2倍,D与氯元素相邻,则D为硫元素;E有2个电子层,最外层电子数为4,则E为碳元素;W是与S同主族的短周期元素,则W为O元素,Z是第三周期金属性最强的元素,则Z为Na,据此分析解答。
(1)融雪剂主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,含有相同的核外电子数,且1molXY2含有54mol电子,则阴、阳离子核外电子数为![]() =18,则为Ca2+、Cl-,故XY2是CaCl2,属于离子化合物,含有离子键,故答案为:CaCl2;离子键;
=18,则为Ca2+、Cl-,故XY2是CaCl2,属于离子化合物,含有离子键,故答案为:CaCl2;离子键;
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与氯元素相邻,则D为硫元素,S2-离子结构示意图是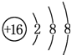 ;则E有2个电子层,最外层电子数为4,则E为碳元素,碳元素与硫元素形成的类似于CO2的三原子分子为CS2,与二氧化碳结构类似,其电子式为
;则E有2个电子层,最外层电子数为4,则E为碳元素,碳元素与硫元素形成的类似于CO2的三原子分子为CS2,与二氧化碳结构类似,其电子式为![]() ,为共价化合物,含有极性共价键,故答案为:
,为共价化合物,含有极性共价键,故答案为: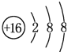 ;
;![]() ;共价键;
;共价键;
(3)W是与S同主族的短周期元素,则W为O元素,Z是第三周期金属性最强的元素,则Z为Na,钠与氧气反应,不加热生成Na2O,属于离子化合物,含有离子键,加热生成Na2O2,属于离子化合物,含有离子键和非极性共价键,电子式为![]() ,故答案为:Na2O;离子键;Na2O2;离子键和非极性共价键;
,故答案为:Na2O;离子键;Na2O2;离子键和非极性共价键;![]() 。
。

【题目】下表是元素周期表的一部分,表中所列的字母分别代表一种元素。
A | |||||||||||||||||
B | C | D | E | F | T | ||||||||||||
G | H | I | J | K | L | ||||||||||||
M | N | O | |||||||||||||||
试回答下列问题(注意:每问中的字母代号为上表中的字母代号,并非为元素符号)
(1)N的单质和水蒸气反应能生成固体X,则I的单质与X反应的化学方程式_______。
(2)D的气态氢化物的VSEPR模型的名称为_______。
(3)由A、C、D形成的ACD分子中,σ键和π键个数比= _______________。
(4)要证明太阳上是否含有R 元素,可采用的方法是__________________________。
(5)元素M的化合物(ME2L2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。回答问题:
①ME2L2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断ME2L2是_________(填“极性”或“非极性”)分子。
②将N和O的单质用导线连接后插入D的最高价氧化物对应的水化物浓溶液中,可制成原电池,则组成负极材料的元素的外围电子轨道表示式为______________________。
(6)往O2+溶液中加入氨水,形成蓝色沉淀,继续加入氨水,难溶物溶解变成蓝色透明溶液,写出沉淀溶解的离子方程式_____。
(7)若F 、K两种元素形成的化合物中中心原子的价电子全部参与成键,则该化合物的空间构型的名称为___。
(8)如图四条折线分别表示ⅣA族、ⅤA族、ⅥA族、ⅦA族元素气态氢化物沸点变化,则E的氢化物所在的折线是__(填m、n、x或y)。

(9)1183 K以下纯N晶体的基本结构单元如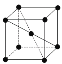 所示,1183 K以上转变为
所示,1183 K以上转变为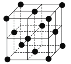 所示结构的基本结构单元。在1183 K以下的晶体中,空间利用率为____;在1183 K以上的晶体中,与N原子等距离且最近的N原子数为____,晶体堆积方式的名称为_____。
所示结构的基本结构单元。在1183 K以下的晶体中,空间利用率为____;在1183 K以上的晶体中,与N原子等距离且最近的N原子数为____,晶体堆积方式的名称为_____。