题目内容
为了用CO2与Na2O2反应来测定不纯Na2O2样品(不含Na2O杂质)的质量分数,请用下列装置设计一个实验:
(1)连接上述装置的正确顺序是(填各接口的字母):I接________,________接________,________接________,________接________,F接________。
(2)使用③号装置的作用是,④号装置的作用是________________________________。
(3)检验⑥号装置中收集的气体的方法是________________,现象是________________。
(4)若反应前称量直玻璃管的质量为100 g,直玻璃管与固体样品总质量为110 g,反应后称量直玻璃管和固体总质量为112.8 g,则样品中Na2O2的质量分数为________。
(1)G H C D A B E J
(2)除去未反应的CO2 除去CO2中的HCl气体
(3)用带火星的木条伸入瓶中 木条复燃
(4)78%
解析:112.8 g-110 g=2.8 g
2Na2O2+2CO2====2Na2CO3+O2 Δm
156 212 56
x 2.8 g
x=7.8 g
w(Na2O2)=![]() ×100%=78%
×100%=78%

 名校课堂系列答案
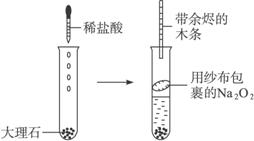
名校课堂系列答案为了探究SO2与Na2O2的反应是否类似于CO2,甲同学设计了如图实验装置。回答下列问题:

(1)移开棉花,将带火星的木条放在C试管口,未见木条复燃。甲同学因此认为SO2与Na2O2的反应不同于CO2。请按甲同学的观点写出反应的化学方程式 。
(2)乙同学认为无论反应原理如何,最终都有O2产生。乙同学的理由是 。
按照乙同学的观点,该装置需作的改进是: 。
(3)假设Na2O2 完全反应,反应后B装置中固体生成物可能是:
① Na2SO3; ② Na2SO4; ③ Na2SO3和Na2SO4
请设计实验方案检验,写出实验步骤以及预期现象和结论,完成下表:
限选试剂:2 mol·L-1 HCl, 1mol·L-1HNO3, 1 mol·L-1 BaCl2, 1 mol·L-1 Ba(NO3)2,
0.01mol·L-1KMnO4酸性溶液。
|
实验步骤 |
预期现象和结论 |
|
步骤1:取B中的少量固体样品于试管中,滴加足量蒸馏水,溶解,然后取少量待测液分别置于Ⅰ、Ⅱ试管中。 |
固体完全溶解 |
|
步骤2:往Ⅰ试管中加入 ,再滴加 。 |
,则证明生成 物中含Na2SO4。 |
|
步骤3:往Ⅱ试管中 。 |
若 , 则说明生成物中有Na2SO3;若 , 则说明生成物中没有Na2SO3。 |
(4)生成物中亚硫酸钠含量的测定:①取a克生成物配制成100ml溶液,取10.00mL该溶液于锥形瓶中,加入几滴淀粉溶液作指示剂,用0.0100mol·L-1碘水进行滴定,滴定终点现象为 ,记录数据,重复滴定2次,平均消耗碘水20.00mL。
②计算:生成物中亚硫酸钠的质量分数为 。(Na2SO3的式量为126)