题目内容
20.对二甲苯(英文名称p-xylene,缩写为PX)是化学工业的重要原料.(1)写出PX的结构简式
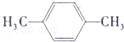 .
.(2)PX可发生的反应有加成反应、取代反应(填反应类型).
(3)增塑剂(DEHP)存在如图所示的转化关系,其中A是PX的一种同分异构体.
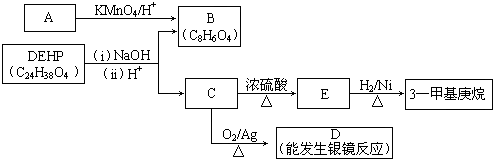
①B的苯环上存在2种等效氢,则B的结构简式是
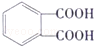 .
.②C分子有1个碳原子连接乙基和正丁基,DEHP的结构简式是
 .
.(4)F是B的一种同分异构体,具有如下特征:
a.是苯的邻位二取代物; b.遇FeCl3溶液显示特征颜色; c.能与碳酸氢钠溶液反应.
写出F与NaHCO3溶液反应的化学方程式
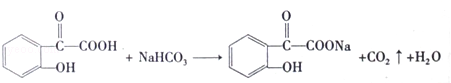 .
.
分析 (1)PX是对二甲苯,其结构简式为 ;
;
(2)PX中含有苯环和甲基,能发生氧化反应、加成反应、取代反应;
(3)(4)A是PX的同分异构体,A被酸性高锰酸钾氧化,生成羧酸,根据B分子式知,A中含有两个甲基,B的苯环上存在2种等效氢,则B的苯环上只有两种氢原子,其结构简式为 ,则A结构简式为
,则A结构简式为 ,DEHP碱性水解然后酸化得到B和C,C中含有醇羟基,根据DEHP和B的分子式知,C是一元醇,C发生消去反应生成E,E与氢气发生加成反应生成3-甲基庚烷,C发生氧化反应生成D,D能发生银镜反应,C分子有1个碳原子连接乙基和正丁基,C为CH3CH2CH2CH2CH(CH2CH3)CH2OH,D为CH3CH2CH2CH2CH(CH2CH3)CHO、E为CH3CH2CH2CH2C(CH2CH3)=CH2,
,DEHP碱性水解然后酸化得到B和C,C中含有醇羟基,根据DEHP和B的分子式知,C是一元醇,C发生消去反应生成E,E与氢气发生加成反应生成3-甲基庚烷,C发生氧化反应生成D,D能发生银镜反应,C分子有1个碳原子连接乙基和正丁基,C为CH3CH2CH2CH2CH(CH2CH3)CH2OH,D为CH3CH2CH2CH2CH(CH2CH3)CHO、E为CH3CH2CH2CH2C(CH2CH3)=CH2,
则DEHP结构简式为 ,据此分析解答.
,据此分析解答.
解答 解:(1)PX是对二甲苯,其结构简式为 ,故答案为:
,故答案为: ;
;
(2)PX中含有苯环和甲基,能发生氧化反应、加成反应、取代反应,
故答案为:加成反应、氧化反应、取代反应(任填两个);
(3)A是PX的同分异构体,A被酸性高锰酸钾氧化,生成羧酸,根据B分子式知,A中含有两个甲基,B的苯环上存在2种等效氢,则B的苯环上只有两种氢原子,其结构简式为 ,则A结构简式为
,则A结构简式为 ,DEHP碱性水解然后酸化得到B和C,C中含有醇羟基,根据DEHP和B的分子式知,C是一元醇,C发生消去反应生成E,E与氢气发生加成反应生成3-甲基庚烷,C发生氧化反应生成D,D能发生银镜反应,C分子有1个碳原子连接乙基和正丁基,C为CH3CH2CH2CH2CH(CH2CH3)CH2OH,D为CH3CH2CH2CH2CH(CH2CH3)CHO、E为CH3CH2CH2CH2C(CH2CH3)=CH2,
,DEHP碱性水解然后酸化得到B和C,C中含有醇羟基,根据DEHP和B的分子式知,C是一元醇,C发生消去反应生成E,E与氢气发生加成反应生成3-甲基庚烷,C发生氧化反应生成D,D能发生银镜反应,C分子有1个碳原子连接乙基和正丁基,C为CH3CH2CH2CH2CH(CH2CH3)CH2OH,D为CH3CH2CH2CH2CH(CH2CH3)CHO、E为CH3CH2CH2CH2C(CH2CH3)=CH2,
则DEHP结构简式为 ,
,
①通过以上分析知,B结构简式为 ,
,
故答案为: ;
;
②通过以上分析知,DEHP的结构简式为 ,
,
故答案为: ;
;
(4)F是B的一种同分异构体,具有如下特征:
a.是苯的邻位二取代物说明含有两个取代基;
b.遇FeCl3溶液显示特征颜色说明含有酚羟基;
c.能与碳酸氢钠溶液反应说明含有羧基,则F结构简式为 .
.
F与NaHCO3溶液反应时只有羧基发生反应,所以该反应的化学方程式为 ,
,
故答案为: .
.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断能力,根据反应条件、物质分子式、结构进行推断,难点是同分异构体种类判断,(5)中酚羟基和碳酸氢钠不反应,为易错点.

| A. | 乙烷 | B. | 甲苯 | C. | 丙炔 | D. | 苯乙烯 |
| A. | 苯能与溴发生取代反应,因此不能用苯萃取溴水中的溴 | |
| B. | 甲烷、苯都属于烃,都不存在同分异构体 | |
| C. | 甲烷和乙烯可以用酸性高锰酸钾溶液鉴别 | |
| D. | 石油的裂解是化学变化,而石油的分馏和煤的干馏都是物理变化 |
 分子中,处于同一平面上的碳原子数最多可能有( )
分子中,处于同一平面上的碳原子数最多可能有( )| A. | 6个 | B. | 8个 | C. | 10个 | D. | 12个 |
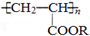 )“水溶液”,“水溶液”中的高分子化合物与沙土粒子结合,在地表下一定深度处形成一个一定厚度的隔水层,既能阻止地下盐分的上升,又有拦截、蓄积雨水的作用.下列关于聚丙烯酸酯的说法正确的是( )
)“水溶液”,“水溶液”中的高分子化合物与沙土粒子结合,在地表下一定深度处形成一个一定厚度的隔水层,既能阻止地下盐分的上升,又有拦截、蓄积雨水的作用.下列关于聚丙烯酸酯的说法正确的是( )| A. | 聚丙烯酸酯是混合物,没有固定的熔沸点 | |
| B. | 聚丙烯酸酯不能发生取代反应 | |
| C. | 聚丙烯酸酯和其单体(单体的结构式为CH2=CHCOOR)都能发生加成反应 | |
| D. | 合成聚丙烯酸酯的反应属于消去反应 |
 运动员服用兴奋剂是违背人文道德的.某种兴奋剂的结构简式如下图所示,有关该物质的说法错误的是( )
运动员服用兴奋剂是违背人文道德的.某种兴奋剂的结构简式如下图所示,有关该物质的说法错误的是( )| A. | 滴入KMnO4(H+)溶液,观察到紫色褪去 | |
| B. | 该分子中的所有碳原子可能共平面 | |
| C. | 1 mol该物质与浓溴水和H2反应最多消耗Br2和H2分别为4 mol、7 mol | |
| D. | 遇FeCl3溶液不显颜色 |
| A. | 分子式是C3H8O3 | |
| B. | A催化氧化的产物能发生银镜反应 | |
| C. | 0.1 mol A与足量Na反应产生2.24 L H2(标准状况) | |
| D. | A在一定条件下发生缩聚反应的产物是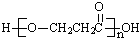 |
[查阅资料]KMnO4溶液氧化H2C2O4的反应历程为:
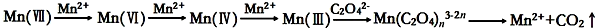
[提出假设]
假设1:该反应为放热反应
假设2:反应生成的Mn2+对该反应有催化作用
假设3:K+对该反应有催化作用
该小组同学未提出浓度使反应速率加快的假设,原因是反应物浓度降低,反应速率减慢.
[设计、完成实验]
(1)称取6.3g草酸晶体(H2C2O4•2H2O),配制500mL0.10mol/L H2C2O4溶液.
①在上述过程中必须用到的2种定量仪器是托盘天平和500mL容量瓶.
②下列操作会使所配溶液浓度偏低的是AD(填下列选项的字母序号).
A.称取草酸晶体时,将草酸晶体放在托盘天平右盘
B.定容时俯视刻度线
C.将烧杯中溶液转移到容量瓶之前,容量瓶中有少量蒸馏水
D.摇匀后,发现溶液液面低于刻度线,立即用胶头滴管加水再定容
(2)完成探究,记录数据
| 实验编号 | 烧杯中所加试剂及用量(mL) | 控制 条件 | 溶液褪色时间(S) | |||
| 0.10mol/LH2C2O4 溶液 | 等浓度 KMnO4溶液 | H2O | 0.50mol/L 稀硫酸 | |||
| 1 | 30 | 20 | 30 | 20 | 18 | |
| 2 | 30 | 20 | 30 | 20 | 水浴控制温度65° | 15 |
| 3 | 30 | 20 | 30 | 20 | 加入少量MnSO4固体 | 3.6 |
| 4 | 30 | 20 | x | 20 | 加入5mL0.10mol/LK2SO4 | 18 |
(3)由于KMnO4能氧化水中有机物等因素,为配制好稳定的KMnO4溶液,其浓度需标定.取10.00mL 0.10mol/L H2C2O4溶液于锥形瓶中,加入10mL 0.50mol/L稀硫酸,用(2)中KMnO4溶液滴定至锥形瓶中恰好呈浅紫色,且半分钟不褪色,记录数据,平行三次实验,平均消耗KMnO4溶液40.00mL,则草酸溶液与酸性KMnO4溶液反应的离子方程式为:5H2C2O4+2MnO4-+6H+=2Mn2++10CO2↑+8H2O.上述实验中KMnO4溶液的物质的量浓度为0.010mol/L.
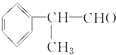 )是一种重要的化工原料,其合成路线如下
)是一种重要的化工原料,其合成路线如下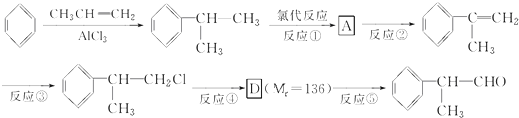
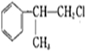 +NaOH$→_{△}^{水}$
+NaOH$→_{△}^{水}$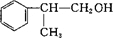 +NaCl.
+NaCl.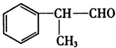 +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$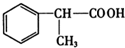 +Cu2O↓+2H2O.
+Cu2O↓+2H2O.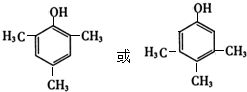 .
.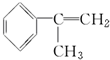 为原料制备
为原料制备 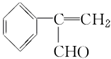 的化学方程式(无机试剂任用).
的化学方程式(无机试剂任用).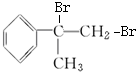 、
、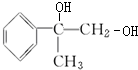 +2NaBr、
+2NaBr、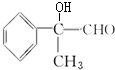 +2H2O、
+2H2O、