题目内容
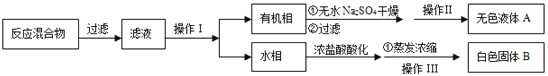
【题目】(10分)将过量Mg粉溶于100mL 1.5mol·L-1稀H2SO4中,反应结束后,滤去多余Mg粉,滤液在t℃下蒸发,当滤液质量为72.0g时开始析出MgSO4·xH2O晶体,当析出晶体12.3g时,剩下滤液48.0g。通过计算请回答下列问题(请写出计算过程)。
(1)生成标准状况下的气体体积;
(2)开始析出MgSO4·xH2O晶体时溶液的质量分数;
(3)MgSO4·xH2O中的x值。
【答案】n(H2SO4)=1.5mol/L![]() 0.1L=0.15mol
0.1L=0.15mol
Mg + H2SO4 = MgSO4 + H2↑
1mol 22.4L
0.15mol V(H2)
![]() =
=![]()
解得V(H2)=3.36L
生成标准状况下气体的体积为3.36L
25% 7
【解析】
(1)n(H2SO4)=1.5mol/L![]() 0.1L=0.15mol
0.1L=0.15mol
Mg + H2SO4 = MgSO4 + H2↑
1mol 1mol 22.4L
0.15mol n(MgSO4)V(H2)
![]() =
=![]() =
=![]()
解得n(MgSO4)=0.15mol V(H2)=3.36L
生成标准状况下气体的体积为3.36L
(2)反应生成的m(MgSO4)=0.15mol![]() 120g/mol=18g,当滤液质量为72.0g时开始析出MgSO4·xH2O晶体,MgSO4饱和溶液(开始析出MgSO4·xH2O晶体时)的质量分数为
120g/mol=18g,当滤液质量为72.0g时开始析出MgSO4·xH2O晶体,MgSO4饱和溶液(开始析出MgSO4·xH2O晶体时)的质量分数为![]() 100%=25%
100%=25%
(3)当析出12.3gMgSO4·xH2O晶体时,剩余滤液48.0g;剩余滤液仍为MgSO4饱和溶液,48.0g滤液中MgSO4的质量为48.0g![]() 25%=12.0g;12.3gMgSO4·xH2O晶体中MgSO4的质量为18g-12.0g=6g,n(MgSO4)=
25%=12.0g;12.3gMgSO4·xH2O晶体中MgSO4的质量为18g-12.0g=6g,n(MgSO4)=![]() =0.05mol,n(H2O)=
=0.05mol,n(H2O)=![]() =0.35mol,n(MgSO4):n(H2O)=1:x=0.05mol:0.35mol,x=7。
=0.35mol,n(MgSO4):n(H2O)=1:x=0.05mol:0.35mol,x=7。

 阅读快车系列答案
阅读快车系列答案【题目】实验室可用溢流法连续制备无水四氯化锡(SnCl4)。SnCl4易挥发,极易发生水解,Cl2极易溶于SnCl4。制备原理与实验装置图如下:
Sn(s)+2Cl2(g)=SnCl4(l) ΔH = –511kJmol-1

可能用到的有关数据如下:
物质 | Sn | SnCl4 | CuCl2 |
熔点/℃ | 232 | -33 | 620 |
沸点/℃ | 2260 | 114 | 993 |
制备过程中,锡粒逐渐被消耗,须提拉橡胶塞及时向反应器中补加锡粒。当SnCl4液面升至侧口高度时,液态产物经侧管流入接收瓶。回答下列问题:
(1)a管的作用是________。
(2)A中反应的离子方程式是________。
(3)D的作用是________。
(4)E中冷却水的作用是________。
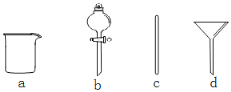
(5)尾气处理时,可选用的装置是________(填序号)。

(6)锡粒中含铜杂质致E中产生CuCl2,但不影响F中产品的纯度,原因是________。
(7)SnCl4粗品中含有Cl2,精制时加入少许锡屑后蒸馏可得纯净的SnCl4。蒸馏过程中不需要用到的仪器有________(填序号)。
A.蒸馏烧瓶 B.温度计 C.接收器 D.冷凝管 E.吸滤瓶