题目内容
13.氯气和水反应生成HCl和HClO,欲从反应混合物中分离出HClO溶液,下列方法可选用的是( )| A. | 加硫酸钙,充分反应后蒸馏 | B. | 加碳酸钙,充分反应后蒸馏 | ||
| C. | 加磷酸钙,充分反应后蒸馏 | D. | 加氯化钙,充分反应后蒸馏 |
分析 氯气与水发生C12+H2O=HCl+HClO,盐酸的酸性比碳酸、磷酸强,HClO的酸性比碳酸、磷酸弱,可加入碳酸钙、磷酸钙除去盐酸,以此解答该题.
解答 解:氯气与水发生C12+H2O=HCl+HClO,盐酸的酸性比碳酸、磷酸强,HClO的酸性比碳酸、磷酸弱,可加入碳酸钙、磷酸钙除去盐酸,题中加入硫酸钙、氯化钙不能除去盐酸,故选BC.
点评 本题考查物质的分离、提纯和除杂等问题,为高频考点,侧重于学生的实验能力的考查,题目难度不大,根据除杂是不能引入新的杂质、不能影响被提纯的物质的性质和量,并且操作简单可行,除杂时要结合物质的物理性质和化学性质进行分离.

练习册系列答案
相关题目
3.如图所示实验操作中,不正确的是( )
| A. |  加热液体 | B. | 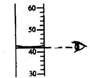 读取液体体积 | C. |  稀释浓硫酸 | D. | 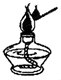 点燃酒精灯 |
4.已知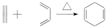 ,如果要合成
,如果要合成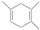 ,所用的起始原料可以是( )
,所用的起始原料可以是( )
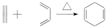 ,如果要合成
,如果要合成 ,所用的起始原料可以是( )
,所用的起始原料可以是( )| A. | 2-甲基-1,3-丁二烯和1-丁炔 | B. | 1,3-戊二烯和2-丁炔 | ||
| C. | 2,3-二甲基-1,3-戊二烯和乙炔 | D. | 2,3-二甲基-1,3-丁二烯和丙炔 |
1.下列离子能在同一溶液中大量共存的是( )
| A. | Ba2+、K+、Cl-、SO42- | B. | K+、H+、Cl-、OH- | ||
| C. | K+、Ag+、Br-、NO3- | D. | Na+、K+、SO42-、OH- |
8.将NO、CO2的混合气体通过装有足量Na2O2的容器后,再用干燥烧瓶收集得到的混合气体,然后倒立于水槽中,最后水充满整个烧瓶,称量Na2O2容器,发现增重28g,则NO的质量是( )
| A. | 14g | B. | 20g | C. | 26g | D. | 28g |
5.向一定量的盐酸中逐滴加入NaAlO2溶液,生成沉淀Al(OH)3的量随NaAlO2加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )

| A. | a点对应的溶液中:NH${\;}_{4}^{+}$、Fe3+、SO${\;}_{4}^{2-}$、HCO${\;}_{3}^{-}$ | |
| B. | b点对应的溶液中:K+、Na+、NO${\;}_{3}^{-}$、Cl- | |
| C. | c点对应的溶液中:Na+、K+、SO${\;}_{4}^{2-}$、OH- | |
| D. | d点对应的溶液中:Ca2+、NH4+、I-、H+ |
13.某温度时,浓度都是2mol/L的两种气体X2和Y2,在密闭容器中反应生成气体Z,达到平衡后c(X2)为0.8mol/L,c(Y2)为1.6mol/L,生成的c(Z)为0.8mol/L,则该反应式(Z用X、Y表示)是( )
| A. | X2+2Y2?2XY2 | B. | 2X2+Y2?2X2Y | C. | X2+3Y2?2XY3 | D. | 3X2+Y2?2X3Y |
14.化学在生产和日常生活中有着重要的应用.下列说法不正确的是( )
| A. | 明矾与水反应成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 | |
| B. | 溶液中溶质粒子能通过滤纸,胶体中分散质粒子不能通过滤纸 | |
| C. | 水泥厂、冶金厂用高压电作用于气溶胶以除去烟尘,是利用了电泳原理 | |
| D. | 江河入海口三角洲的形成通常与胶体的性质有关系 |
