题目内容
【题目】已知还原性:SO32->I-。某溶液X可能含有NH4+、Na+、Ba2+、Fe3+、I-、SO32-、SO42-中的几种,为确定其组成,某同学进行如下实验:
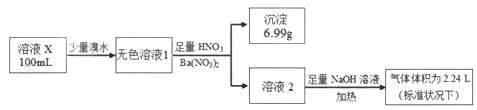
下列说法正确的是
A. 溶液X肯定只存在NH4+、SO42-
B. 溶液X一定不含有Ba2+、Fe3+,可能含有I-
C. 为确定可能存在的阴离子,可另取试液滴加足量盐酸、BaCl2溶液
D. 为确定可能存在的阳离子,可用经过稀硫酸洗过的铂丝蘸取溶液X在酒精灯火焰上灼烧
【答案】C
【解析】某溶液X加入少量溴水,得到无色溶液,说明原溶液一定不含Fe3+、I-,一定含有SO32-,进一步推出一定不含Ba2+;加入硝酸酸化的硝酸钡,生成硫酸钡6.99 g (0.03mol),但不能确定原溶液是否含有SO42-;加入足量氢氧化钠放出氨气2.24L(标准状况),说明原溶液含有0.1 mol NH4+; 根据以上分析,溶液X存在SO32-,故A错误;溶液X一定不含有Ba2+、Fe3+、 I-,故B错误;为确定SO42-可能存在,可另取试液滴加足量盐酸、BaCl2溶液,若生成沉淀则含有SO42-,故C正确;为确定Na+存在,可用经过稀盐酸洗过的铂丝蘸取溶液X在酒精灯火焰上灼烧,故D错误。

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案
相关题目
【题目】下列除杂(括号内是杂质)所选用的试剂及操作方法均正确的一组是( )
选项 | 待提纯的物质 | 选用的试剂 | 操作方法 |
A | CO2(HCl) | 饱和NaHCO3溶液 | 洗气 |
B | Mg(Al) | 过量稀盐酸 | 过滤 |
C | FeCl2溶液(FeCl3) | 足量Fe粉 | 过滤 |
D | CO2(CO) | O2 | 点燃 |
A.A
B.B
C.C
D.D