题目内容
7.若某溶液中加入KSCN溶液后出现红色,则该溶液中还可能大量存在的离子或分子是( )| A. | Na+、K+、S2-、NO3- | B. | Na+、NO3-、SO42-、NH3.H2O | ||
| C. | K+、Ba2+、H2O2、Cl- | D. | Na+、Fe2+、Cl-、SO42- |
分析 某溶液中加入KSCN溶液后出现红色,溶液只含Fe3+,根据离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应等,则离子大量共存,以此来解答.
解答 解:某溶液中加入KSCN溶液后出现红色,溶液只含Fe3+,
A.Fe3+、S2-发生氧化还原反应,不能大量共存,故A错误;
B.Fe3+、NH3.H2O结合生成沉淀,不能大量共存,故B错误
C.Fe3+可促进H2O2分解,不能共存,故C错误;
D.该组离子之间不反应,可大量共存,故D正确;
故选D.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应、氧化还原反应的离子共存考查,题目难度不大.

练习册系列答案
 名题金卷系列答案
名题金卷系列答案 优加精卷系列答案
优加精卷系列答案
相关题目
17.下列变化中,需要加入氧化剂才能实现的是( )
| A. | CO→CO2 | B. | MnO4→Mn2+ | C. | SO2→H2SO3 | D. | NaCl→AgCl |
18.某氢氧化钡溶液中,含 Ba2+ a mol,则OH-的物质的量为( )
| A. | 2amol | B. | a mol | C. | a/2 mol | D. | 4a mol |
15.X、Y、Z、M、W为五种短周期元素.X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15,X与Z可形成XZ2分子;Y与M形成的一种气态化合物能使湿润的红色石蕊试纸变蓝;W的质子数是X、Y、Z、M四种元素质子数之和的1/2.下列说法正确的是( )
| A. | 原子半径:W>Z>Y>X>M | |
| B. | Y2M4和M2Z2的分子中含有不同数目的电子 | |
| C. | X2M2为直线型的共价化合物 | |
| D. | 由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键 |
19.下列各物质中互为同系物的是( )
| A. | 甲醇、乙二醇 | B. | 正丁烷和异丁烷 | C. |  和 和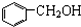 | D. |  和 和 |
16.下列离子方程式中正确的是( )
| A. | 用醋酸除去水垢:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2O | |
| C. | 锌片插入硝酸银溶液中:Zn+Ag+=Zn2++Ag | |
| D. | 碳酸氢铵溶液与足量氢氧化钠溶液反应:NH4++OH-=NH3•H2O |
17.下列物质不属于高分子材料的是( )
| A. | 蛋白质 | B. | 纤维素 | C. | 淀粉 | D. | 油脂 |
 某化学小组为比较盐酸和醋酸的酸性,设计了如下实验方案.装置如图:
某化学小组为比较盐酸和醋酸的酸性,设计了如下实验方案.装置如图: 已知A为常见的金属单质,各物质有如图所示的关系:
已知A为常见的金属单质,各物质有如图所示的关系: