题目内容
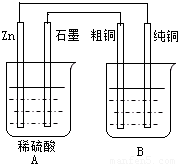
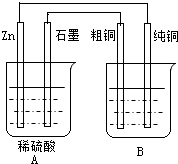
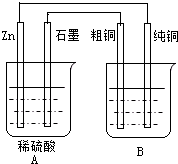 用右图装置能达到粗铜精炼的目的.
用右图装置能达到粗铜精炼的目的.(1)A烧杯是
原电池
原电池
(填〝电解池〞或〝原电池〞),B烧杯是电解池
电解池
(填〝电解池〞或〝原电池〞).(2)其中B烧杯中应该盛
硫酸铜溶液或其它易溶性的铜盐
硫酸铜溶液或其它易溶性的铜盐
溶液.(3)分别写出石墨棒和纯铜棒的电极反应式
石墨棒:
2H++2e-=H2↑
2H++2e-=H2↑
,纯铜棒:
Cu2++2e-=Cu
Cu2++2e-=Cu
.(4)若锌减少了0.65g,则纯Cu的质量增加了多少克?(写出计算过程)
分析:(1)根据原电池和电解池的构成条件来分析;
(2)电解精炼铜时,电解质溶液是含有铜离子的盐;
(3)根据电解池和原电池的工作原理来书写电极反应;
(4)根据电极反应和电子守恒来计算.
(2)电解精炼铜时,电解质溶液是含有铜离子的盐;
(3)根据电解池和原电池的工作原理来书写电极反应;
(4)根据电极反应和电子守恒来计算.
解答:解:(1)A烧杯含有两个活泼性不同的电极,有自发的氧化还原反应,形成了闭合回路,存在电解质溶液,属于原电池装置,B烧杯就存在了外加电源,属于电解装置,故答案为:原电池;电解池;
(2)电解精炼铜时,电解质溶液必须是含有铜离子的可溶性的盐,如硫酸铜溶液或其它易溶性的铜盐等,故答案为:硫酸铜溶液或其它易溶性的铜盐;
(3)石墨棒是原电池的正极,发生电极反应为:2H++2e-=H2↑;纯铜棒是电解池的阴极,
电极反应为:Cu2++2e-=Cu,故答案为:2H++2e-=H2↑;Cu2++2e-=Cu;
(4)在A烧杯中,金属锌电极发生的电极反应为:Zn-2e-→Zn,若锌减少了0.65g即0.01mol时,转移电子为0.02mol,在B烧杯中,纯铜电极发生的反应为:Cu2++2e-→Cu,当转移0.02mol电子时,则析出金属Cu的物质的量为0.01mol,质量为0.64g,
答:纯Cu的质量增加了0.64g.
(2)电解精炼铜时,电解质溶液必须是含有铜离子的可溶性的盐,如硫酸铜溶液或其它易溶性的铜盐等,故答案为:硫酸铜溶液或其它易溶性的铜盐;
(3)石墨棒是原电池的正极,发生电极反应为:2H++2e-=H2↑;纯铜棒是电解池的阴极,
电极反应为:Cu2++2e-=Cu,故答案为:2H++2e-=H2↑;Cu2++2e-=Cu;
(4)在A烧杯中,金属锌电极发生的电极反应为:Zn-2e-→Zn,若锌减少了0.65g即0.01mol时,转移电子为0.02mol,在B烧杯中,纯铜电极发生的反应为:Cu2++2e-→Cu,当转移0.02mol电子时,则析出金属Cu的物质的量为0.01mol,质量为0.64g,
答:纯Cu的质量增加了0.64g.
点评:本题是一道原电池和电解池串联的知识题目,注意电路中转移电子守恒的思想,可以根据所学知识进行回答,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
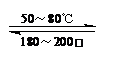 Ni(CO)4(g) 该反应的△H
Ni(CO)4(g) 该反应的△H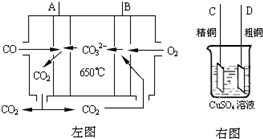
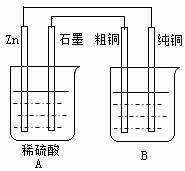 ⑵其中B烧杯中应该盛____ _____溶液。
⑵其中B烧杯中应该盛____ _____溶液。