题目内容
【题目】用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
A.9g甲基(﹣CH3)所含有的电子数是10 NA个
B.22.4L乙烷中含有的共价键数为7NA个
C.常温下,14g乙烯和丙烯的混合物中总原子数为3NA个
D.4.2g C3H6中含有的碳碳双键数一定为0.1NA
【答案】C
【解析】解:A、9g甲基的物质的量为n= ![]() =0.6mol,而甲基不显电性,即1mol甲基中含9mol电子,则0.6mol甲基中含5.4NA个电子,故A错误;
=0.6mol,而甲基不显电性,即1mol甲基中含9mol电子,则0.6mol甲基中含5.4NA个电子,故A错误;
B、乙烯所处的状态不明确,故其物质的量和含有的共价键个数无法计算,故B错误;
C、乙烯和丙烯的最简式均为CH2 , 故14g混合物中含有的CH2的物质的量为1mol,则含3NA个原子,故C正确;
D、C3H6可能为丙烯,也可能为环丙烷,故结构中不一定含碳碳双键,故D错误.
故选C.

练习册系列答案
相关题目
【题目】1000 mL某待测溶液中除含有0.2 mol·L-1的Na+外,还可能含有下列离子中的一种或多种如下表,现进行如下实验操作(每次实验所加试剂均过量):
阳离子 | K+、NH |
阴离子 | Cl-、Br-、CO |
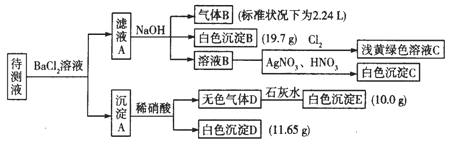
(1)写出生成白色沉淀B的离子方程式:_________。
(2)待测液中肯定不存在的阳离子是_______。
(3)若无色气体D是单一气体:判断原溶液中K+是否存在____(填“是”或“否”),若存在,求其物质的量浓度的最小值,若不存在,请说明理由:__________。
【题目】下列各组关于强电解质、弱电解质、非电解质的归类,完全正确的是( )
A | B | C | D | |
强电解质 | Fe | CaCO3 | NaCl | HNO3 |
弱电解质 | CH3COOH | H3PO4 | NH3 | Fe(OH)3 |
非电解质 | 蔗糖 | 酒精 | BaSO4 | Al2O3 |
A. A B. B C. C D. D