题目内容
在一定温度下,向a L密闭容器中加入1mol X气体和2mol Y气体,发生如下反应:X(g)+2Y(g) 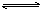 2Z(g),此反应达到平衡的标志是
2Z(g),此反应达到平衡的标志是
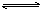 2Z(g),此反应达到平衡的标志是
2Z(g),此反应达到平衡的标志是 | A.容器内气体密度不随时间变化 |
| B.v (X): v (Y)= l:2 |
| C.容器内X、Y、Z的浓度不随时间变化 |
| D.单位时间消耗0.1 molX同时生成0.2molZ |
C
试题分析:在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态,所以选项C正确。密度是混合气的质量和容器容积的比值,在反应过程中质量和容积始终是不变的,所以选项A不能说明。平衡时各种物质的浓度不再发生变化,但各种的浓度之间不一定满足某种关系,C不能说明。D中反应速率的方向是相同,速率之比是相应的化学计量数之比,因此D中的关系始终是成立的,D不能说明,因此答案选C。
点评:该题的关键是明确平衡状态的特点,然后结合具体的可逆反应灵活运用即可,有助于培养学生的逻辑推理能力和发散思维能力。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 xC(g)2min时反应达到平衡状态(温度不变),剩余了0.8molB,并测得C的浓度为0.4mol/L,请填写下列空白:
xC(g)2min时反应达到平衡状态(温度不变),剩余了0.8molB,并测得C的浓度为0.4mol/L,请填写下列空白: nW(g);ΔH,某化学兴趣小组的同学根据此反应在不同条件下的实验数据,作出了如下曲线图:
nW(g);ΔH,某化学兴趣小组的同学根据此反应在不同条件下的实验数据,作出了如下曲线图: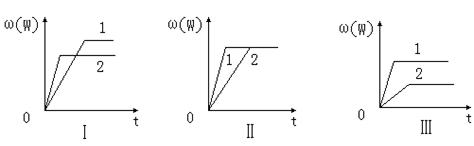
 Z (g)+R (g) ⊿H<0 的气体反应速率(υ)与时间(t)的关系,t1时开始改变条件,则所改变的条件符合曲线的是
Z (g)+R (g) ⊿H<0 的气体反应速率(υ)与时间(t)的关系,t1时开始改变条件,则所改变的条件符合曲线的是
 2NH3(g)+
2NH3(g)+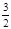 O2(g) △H="+765.0kJ" /mol。
O2(g) △H="+765.0kJ" /mol。
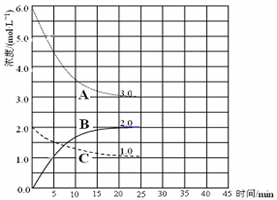
 2C(g)。若经2s后测得C的浓度为0.6 mol/L,现有下列几种说法,其中正确的是( )
2C(g)。若经2s后测得C的浓度为0.6 mol/L,现有下列几种说法,其中正确的是( ) I3-(aq),某I2、KI混合溶液中,c(I3-)与温度T的关系如下图所示(曲线上任何一点都表示平衡状态)。
I3-(aq),某I2、KI混合溶液中,c(I3-)与温度T的关系如下图所示(曲线上任何一点都表示平衡状态)。
 I3-(aq)△H<0
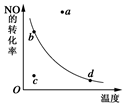
I3-(aq)△H<0  2NO2 △H<0 ,反应中NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是 ( )
2NO2 △H<0 ,反应中NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是 ( )