题目内容
在pH都等于4的HCl和NH4Cl两种溶液中,设由水电离产生的H+ 离子浓度分别为A mol/L与B mol/L,则A和B关系为( )
| A.A>B | B.A=10-6 B |
| C.B=10-6 A | D.A=B |
B
试题分析:pH=4的HCl溶液,由水电离出的c(H+)为10-10,pH=4的NH4Cl溶液,由水电离出的c(H+)为10-4,所以A=10-6 B,答案选B。
点评:盐溶液中盐不能电离出H+,所以盐溶液中的H+都是水电离出来的。

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目

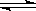 H++OH-,在不同温度下其平衡常数为K(25℃)=1.0×10-14,K(35℃)=2.1×10-14。则下列叙述不正确的是 ( )
H++OH-,在不同温度下其平衡常数为K(25℃)=1.0×10-14,K(35℃)=2.1×10-14。则下列叙述不正确的是 ( )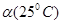 <
<