题目内容
 不锈钢以其优异的抗腐蚀性能越来越受到人们的青睐,它主要是由铁、铬、镍、铜、碳等元素所组成的合金.
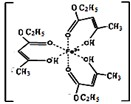
不锈钢以其优异的抗腐蚀性能越来越受到人们的青睐,它主要是由铁、铬、镍、铜、碳等元素所组成的合金.Ⅰ氯化铁溶液用于检验食用香精乙酰乙酸乙酯时,会生成紫色配合物,其配离子结构如图所示.
(1)此配合物中,铁离子的价电子排布式为
(2)此配合物中碳原子的杂化轨道类型有
Ⅱ(1)[Cr (H2O)4Cl2]C1?2H2O中Cr的配位数为
(2)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)n,与Ni(CO)n中配体互为等电子体的离子的化学式为
(3)铜是第四周期最重要的过渡元素之一,其单质及化合物具有广泛用途. CuH的晶体结构如图
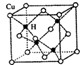 所示,若CuH的密度为d g/cm3,阿伏加德罗常数的值为NA,则该晶胞的边长为
所示,若CuH的密度为d g/cm3,阿伏加德罗常数的值为NA,则该晶胞的边长为分析:I.(1)铁元素是26号元素,铁原子核外有26个电子,铁原子失去3个电子变成铁离子,根据构造原理写出其价电子排布式;
(2)根据碳原子含有的σ键和孤电子对个数确定杂化类型,碳原子的杂化轨道和氢原子的1s轨道形成化学键;
II.(1)根据化学式判断配位数,CrO5中存在过氧键、Cr-O键、Cr=O,在4个Cr-O键中Cr为+1价,在Cr=O键注重Cr为+2价,以此书写结构式;
(2)Ni(CO)4中配体是CO,CO的等电子体是与其原子个数相等且价电子数相等的分子或离子;
(3)利用均摊法计算该晶胞中含有的铜原子和氢原子个数,再根据质量、密度和体积之间的关系式计算,设晶胞的边长为a,a=
;
(2)根据碳原子含有的σ键和孤电子对个数确定杂化类型,碳原子的杂化轨道和氢原子的1s轨道形成化学键;
II.(1)根据化学式判断配位数,CrO5中存在过氧键、Cr-O键、Cr=O,在4个Cr-O键中Cr为+1价,在Cr=O键注重Cr为+2价,以此书写结构式;
(2)Ni(CO)4中配体是CO,CO的等电子体是与其原子个数相等且价电子数相等的分子或离子;
(3)利用均摊法计算该晶胞中含有的铜原子和氢原子个数,再根据质量、密度和体积之间的关系式计算,设晶胞的边长为a,a=
| 3 |
| ||||
解答:解:I.(1)铁元素是26号元素,其原子核外有26个电子,铁原子失去3个电子变成铁离子,其价电子排布式为:3d5,故答案为:3d5;
(2)甲基和乙基上的碳原子含有4个σ键且不含孤电子对,所以采用sp3杂化,碳碳双键两端的碳原子含有3个σ键且不含孤电子对,所以采取杂化sp2,-C2H5中C-H间碳原子的sp3杂化轨道和氢原子的1s轨道形成化学键,
故答案为:sp3、sp2,碳原子的sp3杂化轨道和氢原子的1s轨道;
II.(1)[Cr(H2O)4Cl2]Cl?2H2O中Cr与4个H2O,2个Cl形成配位键,所以配位数为6,CrO5中存在过氧键、Cr-O键、Cr=O,在4个Cr-O键中Cr为+1价,在Cr=O键中Cr为+2价,则结构式为 ,
,
故答案为:6; ;
;
(2)CO分子中含有2个原子,其价电子个数是10,所以与Ni(CO)4中配体互为等电子的离子是CN-、C22-;
故答案为:CN-、C22-;
(4)该晶胞中含有4个H原子,铜原子个数=
×8+6×
=4,所以该晶胞中含有4个铜原子4个氢原子,设该晶胞的边长为a,则a=
=
,故答案为:
.
(2)甲基和乙基上的碳原子含有4个σ键且不含孤电子对,所以采用sp3杂化,碳碳双键两端的碳原子含有3个σ键且不含孤电子对,所以采取杂化sp2,-C2H5中C-H间碳原子的sp3杂化轨道和氢原子的1s轨道形成化学键,
故答案为:sp3、sp2,碳原子的sp3杂化轨道和氢原子的1s轨道;
II.(1)[Cr(H2O)4Cl2]Cl?2H2O中Cr与4个H2O,2个Cl形成配位键,所以配位数为6,CrO5中存在过氧键、Cr-O键、Cr=O,在4个Cr-O键中Cr为+1价,在Cr=O键中Cr为+2价,则结构式为
 ,
,故答案为:6;
 ;
;(2)CO分子中含有2个原子,其价电子个数是10,所以与Ni(CO)4中配体互为等电子的离子是CN-、C22-;
故答案为:CN-、C22-;
(4)该晶胞中含有4个H原子,铜原子个数=
| 1 |
| 8 |
| 1 |
| 2 |
| 3 |
| ||||
| 3 |
| ||
| 3 |
| ||
点评:本题考查较为综合,题目难度较大,涉及晶胞的计算、价电子排布式的书写、等电子体等知识点,晶胞的计算是学习难点,应熟练掌握.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
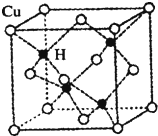 [化学--选修物质结构与性质]不锈钢以其优异的抗腐蚀性能越来越受到人们的青睐,它主要是由铁、铬、镍、铜、碳等元素所组成的合金.
[化学--选修物质结构与性质]不锈钢以其优异的抗腐蚀性能越来越受到人们的青睐,它主要是由铁、铬、镍、铜、碳等元素所组成的合金.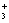 +H2O====C2H5NH2+H3O+
+H2O====C2H5NH2+H3O+