题目内容
【题目】如图中的a和b为氢镍可充电碱性电池的电极,该电池总反应式为2Ni(OH)2![]() H2+2NiO(OH)。
H2+2NiO(OH)。
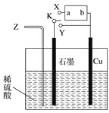
(1)为了实现铜与稀硫酸反应,用Z通入氧气的同时,将开关K与Y相连即可。石墨电极的反应式为______________________________,总反应的化学方程式为________________________________________;
(2)不通入氧气,直接将K与X相连也能实现铜与稀硫酸反应。则氢镍碱性电池的负极为________(填“a”或“b”),电解槽内总反应的离子方程式为_____________________________________________;
(3)当给氢镍碱性电池充电时,该电池的阳极反应式为__________________,氢镍电池放电时,负极附近的pH会________(填“变大”、“不变”或“变小”);
(4)若将图中的稀硫酸换成CuSO4溶液,并且将氢镍碱性电池的电极反接,将K连接X,通电一段时间后,向所得溶液中加入0.2 mol碱式碳酸铜[Cu2(OH)2CO3]后,恰好恢复到原来的浓度和pH(不考虑CO2的溶解),则电解过程中转移电子的物质的量为____________。
【答案】O2+2H2O+4e-=4OH- 2Cu+2H2SO4+O2=2CuSO4+2H2O a Cu+2H+![]() Cu2++H2↑ OH-+Ni(OH)2-e-=NiO(OH)+H2O 变小 1.2 mol
Cu2++H2↑ OH-+Ni(OH)2-e-=NiO(OH)+H2O 变小 1.2 mol
【解析】
(1)石墨电极附近通氧气,则其为正极,发生O2在酸性条件下得电子的反应,总反应为Cu、O2、H2SO4发生氧化还原反应,生成CuSO4和H2O;
(2)不通入氧气,铜仍需失电子,则Cu电极为阳极,与它相连的电极为正极,则另一电极为负极。电解槽内总反应是Cu、H2SO4反应,生成CuSO4和H2;
(3) 氢镍碱性电池的总反应为2Ni(OH)2![]() H2+2NiO(OH),充电时,该电池的阳极是Ni(OH)2在碱性条件下失电子,转化为NiO(OH)。氢镍电池放电时,负极是H2在碱性条件下失电子,消耗OH-生成水;
H2+2NiO(OH),充电时,该电池的阳极是Ni(OH)2在碱性条件下失电子,转化为NiO(OH)。氢镍电池放电时,负极是H2在碱性条件下失电子,消耗OH-生成水;
(4) Cu2(OH)2CO3![]() 2CuO+CO2↑+H2O,则加入0.2 mol碱式碳酸铜[Cu2(OH)2CO3],相当于加入0.4molCuO和0.2molH2O,也即相当于阴极生成0.4molCu和0.2molH2,阳极生成0.3molO2。由此可计算出电解过程中转移电子的物质的量。
2CuO+CO2↑+H2O,则加入0.2 mol碱式碳酸铜[Cu2(OH)2CO3],相当于加入0.4molCuO和0.2molH2O,也即相当于阴极生成0.4molCu和0.2molH2,阳极生成0.3molO2。由此可计算出电解过程中转移电子的物质的量。
(1)石墨电极附近通氧气,则其为正极,在此电极上,O2在酸性条件下得电子,发生反应O2+2H2O+4e-=4OH-;电池中,负极反应为Cu-2e-=Cu2+,则总反应为2Cu+2H2SO4+O2=2CuSO4+2H2O。答案为:O2+2H2O+4e-=4OH-;2Cu+2H2SO4+O2=2CuSO4+2H2O;
(2)不通入氧气,铜仍需失电子,Cu电极为阳极,与它相连的电极b为正极,则另一电极a为负极;电解槽内总反应是Cu、H2SO4生成CuSO4和H2,则反应的离子方程式为Cu+2H+![]() Cu2++H2↑。答案为:a;Cu+2H+
Cu2++H2↑。答案为:a;Cu+2H+![]() Cu2++H2↑;
Cu2++H2↑;
(3)氢镍碱性电池的总反应为2Ni(OH)2![]() H2+2NiO(OH),充电时,该电池的阳极是Ni(OH)2在碱性条件下失电子,转化为NiO(OH),电极反应式为OH-+Ni(OH)2-e-=NiO(OH)+H2O。氢镍电池放电时,负极是H2-2e-+2OH-=2H2O,消耗OH-,从而使溶液的pH变小。答案为:OH-+Ni(OH)2-e-=NiO(OH)+H2O;变小;
H2+2NiO(OH),充电时,该电池的阳极是Ni(OH)2在碱性条件下失电子,转化为NiO(OH),电极反应式为OH-+Ni(OH)2-e-=NiO(OH)+H2O。氢镍电池放电时,负极是H2-2e-+2OH-=2H2O,消耗OH-,从而使溶液的pH变小。答案为:OH-+Ni(OH)2-e-=NiO(OH)+H2O;变小;
(4) Cu2(OH)2CO3![]() 2CuO+CO2↑+H2O,则加入0.2 mol碱式碳酸铜[Cu2(OH)2CO3],相当于加入0.4molCuO和0.2molH2O,也即相当于阴极生成0.4molCu和0.2molH2,阳极生成0.3molO2,用O2计算,可求出电解过程中转移电子的物质的量为0.3mol×[0-(-2)]×2=1.2mol。
2CuO+CO2↑+H2O,则加入0.2 mol碱式碳酸铜[Cu2(OH)2CO3],相当于加入0.4molCuO和0.2molH2O,也即相当于阴极生成0.4molCu和0.2molH2,阳极生成0.3molO2,用O2计算,可求出电解过程中转移电子的物质的量为0.3mol×[0-(-2)]×2=1.2mol。
答案为:1.2 mol。

 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案【题目】某化学兴趣小组制取氯酸钾和氯水并进行有关探究实验。
实验一 制取氯酸钾和氯水
利用如图所示的实验装置进行实验。

(1)制取实验结束后,取出B中试管冷却结晶,过滤,洗涤。该实验操作过程需要的玻璃仪器有______。
(2)若对调B和C装置的位置,_____(填“可能”或“不可能”)提高B中氯酸钾的产率。
实验二 氯酸钾与碘化钾反应的研究
(3)在不同条件下KClO3可将KI氧化为I2或KIO3。该小组设计了系列实验研究反应条件对反应产物的影响,其中系列a实验的记录表如下(实验在室温下进行):
试管编号 | 1 | 2 | 3 | 4 |
0.20molL-1KI/mL | 1.0 | 1.0 | 1.0 | 1.0 |
KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
6.0molL-1H2SO4/mL | 0 | 3.0 | 6.0 | 9.0 |
蒸馏水/mL | 9.0 | 6.0 | 3.0 | 0 |
实验现象 |
①系列a实验的实验目的是______。
②设计1号试管实验的作用是______。
③若2号试管实验现象是溶液变为黄色,取少量该溶液加入______溶液显蓝色。
实验三 测定饱和氯水中氯元素的总量
(4)根据下列资料,为该小组设计一个简单可行的实验方案(不必描述操作过程的细节):_____。
资料:①次氯酸会破坏酸碱指示剂;
②次氯酸或氯水可被SO2、H2O2和FeCl2等物质还原成Cl-。