题目内容
【题目】下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。

完成下列填空(填元素符号或化学式):
(1)元素B在元素周期表中的位置是第____周期第_____族,A、B、C三种元素原子半径从大到小的顺序是_________________;
(2)D简单离子的结构示意图为_____________,D、E中金属性较强的元素是________。D单质在空气中燃烧可生成淡黄色粉末X(D2O2),X常用作呼吸面具和潜水艇中的供氧剂,可选用合适的化学试剂和下图所示实验装置证明X有提供氧气的作用。
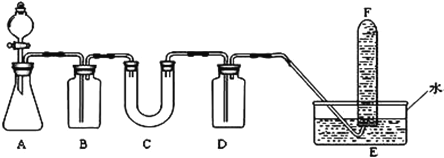
(3)装置A使用石灰石与浓盐酸反应制取CO2,装置B中饱和NaHCO3溶液的作用是除去_____________;
(4)装置C中X与CO2反应的化学方程式是_____________________,装置D盛放NaOH溶液的作用是除去____________;
(5)为检验试管F收集的气体,进行____________操作,出现_________现象,即证明X可作供氧剂。
【答案】二 VA N>O>H ![]() Na HCl 2Na2O2+2CO2=2Na2CO3+O2 CO2 将带火星的木条靠近气体 木条复燃
Na HCl 2Na2O2+2CO2=2Na2CO3+O2 CO2 将带火星的木条靠近气体 木条复燃
【解析】
根据题给的部分元素周期表,明确A、B、C、D、E分别为H、N、O、Na、Mg等元素。用好元素周期律进行原子半径、金属性强弱的判断即可。
(1)根据题给图示,元素B在元素周期表的第二行,从左数第5种元素,所以其在元素周期表的位置表达为第2周期第VA族;元素A、B、C分别为H、N、O,它们的原子半径的从大到小顺序为:N>O>H;
(2)元素D为钠元素,其简单离子的电子式表达为:![]() ,注意看清是离子;元素E为Mg元素,金属性Na>Mg;钠在氧气中燃烧生成的淡黄色粉末为Na2O2;
,注意看清是离子;元素E为Mg元素,金属性Na>Mg;钠在氧气中燃烧生成的淡黄色粉末为Na2O2;
(3)浓盐酸具有强的挥发性,所以制得的CO2气体中混有大量的氯化氢气体,装置B中饱和NaHCO3溶液的作用是除去挥发出的HCl:NaHCO3+HCl=NaCl+H2O+CO2↑,既除去了HCl,又生成了主要成分CO2,又降低了CO2气体在溶液中的溶解损耗;
(4)Na2O2与CO2反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2;装置D盛放NaOH溶液的作用是除去O2中未反应的CO2;
(5)为检验试管F收集的气体是氧气,可用带火星的木条进行检验,如果木条复燃,说明收集到的是O2,从而说明过氧化钠能与二氧化碳反应生成O2,可用作供氧剂。

【题目】某实验小组欲探究Na2CO3和NaHCO3的性质,发现实验室里盛放两种固体的试剂瓶丢失了标签.于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究.
(1)分别加热固体A、B,发现固体A受热产生的气体能使澄清石灰水变浑浊.A受热分解的化学方程式为_____.
(2)称取两种固体各2g,分别加入两个小烧杯中,再各加10mL 蒸馏水,振荡,恢复至室温,发现Na2CO3固体完全溶解,而NaHCO3固体有剩余,由此得出结论_____.
(3)如图所示,在气密性良好的装置Ⅰ和Ⅱ中分别放入药品,将气球内的固体同时倒入试管中.
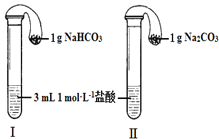
①两试管中均产生气体,_____(填“Ⅰ”或“Ⅱ”)的反应程度更为剧烈.
②反应结束后,气球均有膨胀,恢复至室温,下列说法正确的是_____.
a 装置 I的气球体积较大 b 装置Ⅱ的气球体积较大
c 装置 I的气球体积等于装置Ⅱ的气球体积 d 无法判断
(4)同学们将两种固体分别配制成0.5molL﹣1的溶液,设计如下方案并对反应现象做出预测:
实验方案 | 预测现象 | 预测依据 |
操作1:向2mL Na2CO3溶液中滴加1mL 0.5molL﹣1CaCl2溶液 | 有白色沉淀 | Na2CO3溶液中的CO32﹣浓度较大,能与CaCl2发生反应__________(写离子方程式). |
操作2:向2mL NaHCO3溶液中滴加1mL 0.5molL﹣1CaCl2溶液 | 无白色沉淀 | Na2CO3溶液中的CO32﹣浓度很小,不能与CaCl2发生反应。 |
操作1反应的离子方程式为________________,实施试验后,发现操作2的现象与预测有差异,产生白色沉淀和气体,则该条件下,NaHCO3溶液与CaCl2溶液反应的离子方程式为____________.