题目内容
(6分)发射卫星时可用肼(N2H4)为燃料和二氧化氮做氧化剂,两者反应生成氮气和气态水。
已知: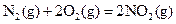 △H=+67.7k
△H=+67.7k J·mol-1
J·mol-1
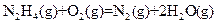 △H=-543kJ·mol-1
△H=-543kJ·mol-1
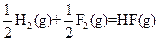 △H=-269kJ·mol-1
△H=-269kJ·mol-1
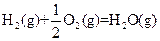 △H=-242kJ·mol-1
△H=-242kJ·mol-1
(1)肼和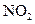 反应的热化学方程式为: 。
反应的热化学方程式为: 。
(2)有人认为若用氟气代替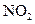 作氧化剂,则反应释放的能量更大,肼和氟气反应的热化学方程式为: 。
作氧化剂,则反应释放的能量更大,肼和氟气反应的热化学方程式为: 。
已知:
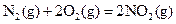 △H=+67.7k
△H=+67.7k J·mol-1
J·mol-1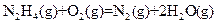 △H=-543kJ·mol-1
△H=-543kJ·mol-1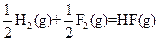 △H=-269kJ·mol-1
△H=-269kJ·mol-1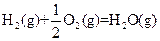 △H=-242kJ·mol-1
△H=-242kJ·mol-1(1)肼和
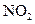 反应的热化学方程式为: 。
反应的热化学方程式为: 。(2)有人认为若用氟气代替
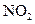 作氧化剂,则反应释放的能量更大,肼和氟气反应的热化学方程式为: 。
作氧化剂,则反应释放的能量更大,肼和氟气反应的热化学方程式为: 。①2N2H4(g) + 2NO2(g) =" " 3N2(g) + 4H2O(g) ΔH = -1153.7 kJ·mol-1
②N2H4(g) + 2F2(g) =" " N2(g) + 4HF(g) ΔH = -1135 kJ·mol-1
ΔH = -1135 kJ·mol-1
②N2H4(g) + 2F2(g) =" " N2(g) + 4HF(g)
 ΔH = -1135 kJ·mol-1
ΔH = -1135 kJ·mol-1 略

练习册系列答案
相关题目




 CO(g)+H2(g) ΔH=+131.3 kJ?mol-1,ΔS=+133.7J?(K?mol) -1
CO(g)+H2(g) ΔH=+131.3 kJ?mol-1,ΔS=+133.7J?(K?mol) -1  CO(g)+H2O(g) CO2(g)+H2(g),得到如下三组数据:
CO(g)+H2O(g) CO2(g)+H2(g),得到如下三组数据:
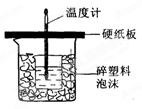
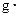 ℃),盐酸和NaOH溶液的密度认为都是1
℃),盐酸和NaOH溶液的密度认为都是1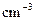 )
)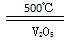 2SO3△H=-196.6kJ·mol-1
2SO3△H=-196.6kJ·mol-1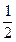 O2(g)====H2O(l)△H=-285.8kJ·mol-1
O2(g)====H2O(l)△H=-285.8kJ·mol-1