题目内容
下列各组物质中,将前者加入后者时,无论前者是否过量,都能用一个离子方程式表示的是( )A.稀盐酸、Na2CO3溶液 B.AlCl3溶液、氨水
C.NH4HSO4溶液、Ba(OH)2溶液 D.浓氨水、硝酸银溶液
B
解析:盐酸加入到碳酸钠中,当盐酸不足时,生成氯化钠和碳酸氢钠,当盐酸足量时生成氯化钠、水和二氧化碳;氨水加入到氯化铝中,不管氨水是否过量都生成氯化铵和氢氧化铝沉淀;硫酸氢铵加入到氢氧化钡中,因为氢氧化钡先于硫酸氢铵中的H+反应完后,再与硫酸氢铵中的![]() 反应,所以当硫酸氢铵不足时生成硫酸钡沉淀、水和氨气,当硫酸氢铵足量时生成硫酸铵、硫酸钡和水;浓氨水滴入硝酸银溶液中,当氨水较少时生成氢氧化银沉淀,当较多时生成银氨络离子。
反应,所以当硫酸氢铵不足时生成硫酸钡沉淀、水和氨气,当硫酸氢铵足量时生成硫酸铵、硫酸钡和水;浓氨水滴入硝酸银溶液中,当氨水较少时生成氢氧化银沉淀,当较多时生成银氨络离子。

练习册系列答案
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案
相关题目
I.可用于分离或提纯物质的方法有:
A.蒸馏;B.盐析;C.过滤;D.重结晶;E、升华;F、渗析;G、电解;H、加热分解;I.洗气.如欲分离或提纯下列各组混合物,请选择上述方法中最合适者,并将相应字母填入题后空格内:
(1)除去淀粉溶液中的少量碘化钠______;
(2)从油脂皂化反应后的混合液中分离出高级脂肪酸钠______;
(3)除去粗铜中锌、银等金属______;
(4)除去水中的Na+、S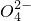 、Cl-等杂质______;
、Cl-等杂质______;
(5)除去KNO3晶体中混有的少量NaCl______.
II.某学生完成硫酸铜晶体结晶水含量测定实验得到以下数据:
| 加热前质量 | 加热前质量 | 加热后质量 |
| W1(容器) | W2(容器+晶体) | W3(容器+无水硫酸铜) |
III.50mL0.50mol?L-1盐酸和50mL 0.55mol?L-1烧碱溶液进行中和反应,若三次平行操作测得数据中起始时盐酸与烧碱溶液平均温度相同,而终止温度与起始温度差(t2-t1)分别为①2.3℃②2.4℃③2.9℃,则△H=______KJ/mol(填数学计算式).[反应后混合液的比热容为4.18J/(g?℃)].







 B、
B、
 D、
D、