题目内容
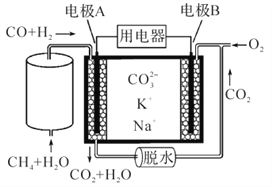
【题目】一种新型熔融碳酸盐燃料电池原理示意如图。下列有关该电池的说法正确的是 ( )
A. 催化重整中CH4+H2O=3H2+CO,1 mol CH4参加反应转移2 mol电子
B. 电极A上H2参与的电极反应为:H2+2OH--2e-=2H2O
C. 电池工作时,CO32-向电极B移动
D. 电极B上的电极反应:O2+2CO2+4e- =2CO32-
【答案】D
【解析】试题分析:由图可知,该装置为原电池,电池反应为一氧化碳、氢气分别与氧气反应生成二氧化碳和水。A电极为负极、B电极为正极,A. 催化重整中CH4+H2O=3H2+CO,碳元素的化合价从-4升高到+2,升高了6价,所以1 mol CH4参加反应转移6 mol电子,A不正确;B. 电极A上H2参与的电极反应为:H2+ CO32--2e-=H2O+ CO2,B不正确;C. 电池工作时,阴离子向负极定向移动,所以CO32-向电极A移动,C不正确;D. 电极B上的电极反应为O2+2CO2+4e- =2CO32-,D正确。本题选D。

练习册系列答案
相关题目