题目内容
常温下,向20mL浓度为0.1000mol/L的盐酸中逐滴加入0.1000mol/L的氨水,PH随氨水体积的变化如图。下列说法不正确的是
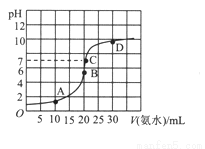
A. 在B点时:c(H+)=c(OH-)+c(NH3·H2O)
B. 在C点时:c(Cl-)<c(NH4+)+c(NH3·H2O)
C. A点与B点相比:2n(NH4+)A>n(NH4+)B
D. 从C到D的过程中,可能出现:c(Cl-)>c(NH4+)
练习册系列答案
相关题目
下列有关物质的性质与用途具有对应关系的是
性质 | 用途 | |
A | 液氨气化吸热 | 可用作制冷剂 |
B | NH4HCO3受热易分解 | 可用作氮肥 |
C | 二氧化硅能与HF反应 | 可用作光导纤维 |
D | 二氧化硫能使溴水褪色 | 可用作漂白剂 |
A. A B. B C. C D. D
一定温度下,向3个初始体积均为1.0 L的密闭容器中按下表所示投料,发生反应N2(g)+3H2(g) 2NH3(g) △H<0达到平衡,下列说法错误的是
2NH3(g) △H<0达到平衡,下列说法错误的是
容器编号 | 容器类型 | 起始物质的量/mol | 反应物的转化率 | 平衡时NH3的物质的量/mol | ||
N2 | H2 | NH3 | ||||
Ⅰ | 恒温恒容 | 1 | 3 | 0 | α1 | 1.2 |
Ⅱ | 绝热恒容 | 1 | 3 | 0 | α2 | a |
Ⅲ | 恒温恒压 | 2 | 6 | 0 | α3 | b |
A. 达到平衡时,α1>α2
B. 平衡时NH3的物质的量b<2.4
C. 达到平衡时,容器Ⅱ中的反应速率比容器Ⅰ中的大
D. 保持温度不变,向容器Ⅰ中再充入0.1mol N2、0.2mol H2、0.2 mol  NH3,平衡向正反应方向移动
NH3,平衡向正反应方向移动