ƒøƒ⁄»ð
°æƒø°øªØ—ß∂‘»À¿ý…Áª·Ω¯≤Ω∫Õ∑¢’πµƒπ±œ◊÷Æ“ª «∑¢œ÷∫Õ—–÷∆¡À∏˜÷÷≤ƒ¡œ£¨¿˝»Á£¨Ω ÙæÕ «Œ“√«…˙ªÓ÷–≤ªø…ªÚ»±µƒ÷ÿ“™≤ƒ¡œ£¨∏˘æðƒ„—ßπ˝µƒ”–πÿΩ Ùµƒ÷™ ∂£¨ªÿ¥œ¬¡–Œ £∫
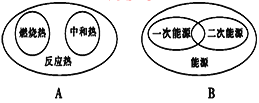
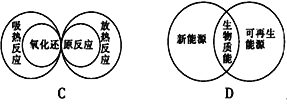
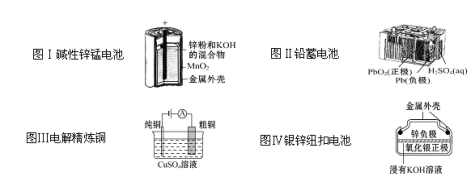
£®1£©Õ≠«Æ‘⁄Œ“π˙¿˙ ∑…œ‘¯æ≠ «“ª÷÷π„∑∫¡˜Õ®µƒªı±“£¨Õ≠≥£”√”⁄÷∆‘Ϫı±“µƒ‘≠“Úø…ƒÐ «_______ÃÓ–Ú∫≈£©°£
A£ÆÕ≠µƒ»€µ„≤ª «Ã´∏þ£¨“◊”⁄“±¡∂£¨÷˝‘Ï≥…–Õ
B£ÆÕ≠µƒ–‘÷ ≤ªªÓ∆√£¨≤ª“◊±ª∏Ø ¥
C£ÆŒ“π˙Ωœ‘Áµƒ’∆Œ’¡À ™∑®“±¡∂Õ≠µƒºº ı
D£Æ◊‘»ªΩÁ”–¥Û¡øµƒ”Œ¿Î赃Õ≠
£®2£©∏÷Ã˙÷∆∆∑µƒ π”√∏¸Œ™π„∑∫£¨µ´ «Ã˙÷∆∆∑“◊…˙–‚£¨Ã˙–‚µƒ÷˜“™≥…∑÷ «_______£®ÃÓ√˚≥∆£©£¨Ã˙µƒ—ıªØŒÔ≥£º˚µƒªπ”–_______°¢_______£®ÃÓªØ—ß Ω£©°£
£®3£©¬¡÷∆∆∑“ÚŒ™±Ì√Ê“◊–Œ≥…÷¬√еƒ—ıªØ¬¡±°ƒ§∂¯æ≠æ√ƒÕ”√£¨µ´ «∏√—ıªØƒ§“◊±ªÀ·ºÓ∆∆ªµ£¨»Ù π—ıªØ¬¡”Ηı—ıªØƒ∆»Ð“∫◊˜”√£¨∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™_____£¨¿Î◊”∑Ω≥Ã ΩŒ™______°£

°æ¥∞∏°øABC»˝—ıªØ∂˛Ã˙FeOFe3O4Al2O3+2NaOH£Ω2NaAlO2+H2OAl2O3+2OH£≠£Ω2AlO2£≠+H2O
°æΩ‚Œˆ°ø
£®1£©A£ÆÕ≠µƒ»€µ„≤ª «Ã´∏þ£¨“◊”⁄“±¡∂°¢÷˝‘Ï≥…–Õ£¨ø…”¶”√”⁄÷∆‘Ϫı±“£¨A’˝»∑£ª
B£ÆÕ≠µƒ–‘÷ ≤ªªÓ∆√£¨≤ª”Îø’∆¯÷–µƒÀÆ—ı∆¯µ»∑¥”¶£¨≤ª“◊±ª∏Ø ¥£¨B’˝»∑£ª
C£ÆŒ“π˙Ωœ‘Áµƒ’∆Œ’¡À ™∑®“±¡∂Õ≠µƒºº ı£¨¿˚”√Fe”ΡÚÀ·Õ≠∑¥”¶…˙≥…Cu£¨C’˝»∑£ª
D£Æ◊‘»ªΩÁ”–¥Û¡øÕ≠øÛ£¨ø™≤…∫Û÷¡∂Cu£¨D¥ÌŒÛ£ª
¥∞∏—°ABC£ª
£®2£©Ã˙÷∆∆∑“◊…˙–‚£¨Ã˙–‚µƒ÷˜“™≥…∑÷ «»˝—ıªØ∂˛Ã˙£ª≥£º˚Ã˙µƒ—ıªØŒÔ”–FeO°¢Fe3O4£ª
£®3£©—ıªØ¬¡ «¡Ω–‘—ıªØŒÔ£¨”Ϋ‚—ıªØƒ∆»Ð“∫∑¥”¶…˙≥…∆´¬¡À·ƒ∆∫ÕÀÆ£¨ªØ—ß∑Ω≥Ã ΩŒ™Al2O3+2NaOH£Ω2NaAlO2+H2O£¨¿Î◊”∑Ω≥Ã ΩŒ™Al2O3+2OH£≠£Ω2AlO2£≠+H2O°£

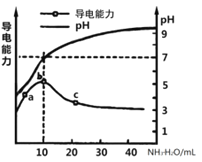
°æƒø°øÀ·–‘ KMnO4 »Ð“∫ƒÐ”Î≤ðÀ·(H2C2O4)»Ð“∫∑¥”¶°£ƒ≥ªØ—ßÃΩæø–°◊È¿˚”√∑¥”¶π˝≥Ã÷–»Ð“∫◊œ…´œ˚ ßøϬ˝µƒ ∑Ω∑®¿¥—–æø”∞œÏ∑¥”¶ÀŸ¬ µƒ“ÚÀÿ°£
I. µ—È«∞ ◊œ»”√≈®∂»Œ™ 0.1000 mol/L À·–‘ KMnO4 ±Í◊º»Ð“∫µŒ∂®Œ¥÷™≈®∂»µƒ≤ðÀ·»Ð“∫°£
£®1£©–¥≥ˆµŒ∂®π˝≥Ã÷–∑¢…˙∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω °£
£®2£©œ¬¡–”–πÿ“ª∂®ŒÔ÷ µƒ¡ø≈®∂»»Ð“∫≈‰÷∆µƒÀµ∑®÷–’˝»∑µƒ « °£
A£Æ∞— 15.8 g KMnO4 πÃûД⁄ 1 L ÀÆ÷–À˘µ√»Ð“∫ŒÔ÷ µƒ¡ø≈®∂»Œ™ 0.1 mol/L
B£Æ∞— 0.01 mol KMnO4 πÃÃÂÕ∂»Î 100 mL »ð¡ø∆ø÷–º”ÀÆ÷¡øÃ∂»œþ£¨≥‰∑÷’Òµ¥∫Û£¨≈®∂»Œ™ 0.1 mol/L
C£Æ–Ë“™ 90 mL 0.1 mol/L µƒ KMnO4 »Ð“∫£¨”¶◊º»∑≥∆¡ø KMnO4 πÃà1 58 g
D£Æ∂®»ð ±—ˆ ”»ð¡ø∆øæ±øÃ∂»œþ∂¡ ˝£¨ª· π≈‰÷∆µƒ»Ð“∫≈®∂»∆´∏þ
II.Õ®π˝µŒ∂® µ—ȵ√µΩ≤ðÀ·»Ð“∫µƒ≈®∂»Œ™ 0.2000 mol/L°£”√∏√≤ðÀ·»Ð“∫∞¥œ¬±ÌΩ¯––∫Û–¯ µ—È(√ø¥Œ µ—È≤ðÀ·»Ð“∫µƒ”√¡øæ˘Œ™ 8.00 mL)°£
µ—ȱý∫≈ | Œ¬∂»(°Ê) | ¥þªØº¡”√¡ø(g) | À·–‘∏þ√ÃÀ·ºÿ »Ð“∫ | |
ê˝(mL) | ≈®∂»(mol/L) | |||
1 | 25 | 0.5 | 4.00 | 0.1000 |
2 | 50 | 0.5 | 4.00 | 0.1000 |
3 | 25 | 0.5 | 4.00 | 0.0100 |
4 | 25 | 0 | 4.00 | 0.1000 |
£®3£©–¥≥ˆ±Ì÷– µ—È 1 ∫Õ µ—È 2 µƒ µ—ȃøµƒ£∫ °£
£®4£©∏√–°◊ÈÕ¨—ß∂‘ µ—È 1 ∫Õ µ—È 3 ∑÷±Ω¯––¡À»˝¥Œ µ—È£¨≤‚µ√“‘œ¬ µ—È ˝æð(¥”ªÏ∫œ’Òµ¥æ˘‘»ø™ ºº∆ ±)£∫
µ—È ±ý∫≈ | »Ð“∫Õ …´À˘–Ë ±º‰ (min) | ||
µ⁄ 1 ¥Œ | µ⁄ 2 ¥Œ | µ⁄ 3 ¥Œ | |
1 | 14.0 | 13.0 | 11.0 |
2 | 6.5 | 6.7 | 6.8 |
∑÷Œˆ…œ ˆ ˝æð∫Ûµ√≥ˆ°∞∆‰À˚Ãıº˛œýÕ¨ ±£¨À·–‘∏þ√ÃÀ·ºÿ»Ð“∫µƒ≈®∂»‘Ω–°£¨Õ …´ ±º‰æÕ‘Ω∂㨺¥∑¥”¶ÀŸ¬ æÕ‘ΩøÏ°±µƒΩ·¬€°£º◊Õ¨—ß»œŒ™∏√–°◊È°∞ÃΩæø∑¥”¶ŒÔ≈®∂»∂‘ÀŸ¬ ”∞œÏ°±µƒ µ—È∑Ω∞∏…˺∆÷–¥Ê‘⁄Œ £¨¥”∂¯µ√µΩ¡À¥ÌŒÛµƒ µ—ÈΩ·¬€£¨º◊Õ¨—ß∏ƒΩ¯¡À µ—È∑Ω∞∏£¨«ÎºÚ ˆº◊Õ¨—ß∏ƒΩ¯ µƒ µ—È∑Ω∞∏______________°£
£®5£©∏√ µ—È÷– π”√µƒ¥þªØº¡”¶—°‘Ò MnSO4 ≤¢∑« MnCl2£¨‘≠“Úø…”√¿Î◊”∑Ω≥Ã Ω±Ì æŒ™________°£
III.𧓵…œø…”√»Ì√ÃøÛ(÷˜“™≥…∑÷Œ™ MnO2)æ≠œ¬¡–…˙≤˙π˝≥Ã÷∆±∏∏þ√ÃÀ·ºÿ°£
¢Ÿ”…»Ì√ÃøÛ÷»°µ√µΩ MnO2£¨»ª∫Û‘⁄ MnO2°¢KOH µƒ»€»⁄ªÏ∫œŒÔ÷–Õ®»Îø’∆¯ø…÷∆µ√√ÃÀ·ºÿ(K2MnO4)£ª
¢⁄œÚ√ÃÀ·ºÿ»Ð“∫÷–Õ®»ÎCO2ø…ªÒµ√∏þ√ÃÀ·ºÿ°£
£®6£©µ⁄¢Ÿ≤Ω…˙≤˙π˝≥Ã÷–£¨‘⁄»€»⁄ªÏ∫œŒÔ÷–Õ®»Îø’∆¯ ±∑¢…˙∑¥”¶µƒªØ—ß∑Ω≥Ã Ω£∫______________°£
£®7£©œÚ√ÃÀ·ºÿ»Ð“∫÷–Õ®»ÎCO2ø…ªÒµ√∏þ√ÃÀ·ºÿ£¨∏√∑¥”¶÷–—ıªØ≤˙ŒÔ”Ϊπ‘≠≤˙ŒÔµƒŒÔ÷ µƒ¡ø÷Ʊ»Œ™________________°£