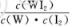题目内容
下列关于氯水的叙述正确的是
- A.氯水中只存在一种电离平衡
- B.向氯水中通入SO2,其漂白性增强
- C.向饱和氯水中通入氯气,c(H+)/c(ClO一)减小
- D.向氯水中加入NaOH至中性,溶液中c(Na+)=c(Cl一)+c(CIO一)
D
A错误,氯水中除了次氯酸这种弱电解质的电离平衡外,还有水的电离平衡。
B错误,氯水可以将二氧化硫氧化,两者都失去漂白性。
C错误,由于氯水已经是饱和状态,所以继续通入氯气不会影响各微粒浓度。
D正确,可以通过电荷守恒推知。
A错误,氯水中除了次氯酸这种弱电解质的电离平衡外,还有水的电离平衡。
B错误,氯水可以将二氧化硫氧化,两者都失去漂白性。
C错误,由于氯水已经是饱和状态,所以继续通入氯气不会影响各微粒浓度。
D正确,可以通过电荷守恒推知。

练习册系列答案
相关题目
运用化学反应原理研究卤族元素的有关性质具有重要意义.
(1)下列关于氯水的叙述正确的是______(填写序号).
a.氯水中存在两种电离平衡
b.向氯水中通入SO2,其漂白性增强
c.向氯水中通入氯气,c(H+)/c(ClO-)减小
d.加水稀释氯水,溶液中的所有离子浓度均减小
e.加水稀释氯水,水的电离平衡向正反应方向移动
f.向氯水中加少量固体NaOH,可能有c(Na+)=c(Cl-)+c(ClO-)
(2)氯气在工业上有着极其广泛的用途.工业上通过氯碱工业生产氯气,其反应的离子方程式为______.用惰性电极电解100mL饱和食盐水,当阴极产生标准状况下11.2mL气体,忽略溶液体积的变化时,所得溶液的pH=______.
(3)常温下,已知25℃时有关弱酸的电离平衡常数:
| 弱酸化学式 | HClO | H2CO3 |
| 电离平衡常数 | K=4.7×10-8 | K1=4.3×10-7,K2=5.6×10-11 |
(4)服用含碘化钾的碘药片可抗核辐射.将碘药片剥去糖衣皮研碎后置于试管中制得无色水溶液,并加入几滴淀粉试液,然后向试管中逐滴加入氯水,观察到溶液由无色变为蓝色,若继续滴加氯水后蓝色溶液又褪为无色.写出化学反应方程式:______.